ОРИГИНАЛЬНЫЕ СТАТЬИ
Цель: оценить влияние комплексной реабилитации на динамику изменения антропометрических показателей пациенток после радикального хирургического лечения ранних стадий рака яичников (РЯ).
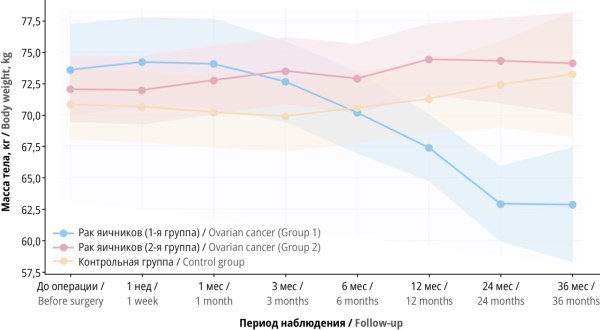
Материал и методы. В проспективное рандомизированное контролируемое исследование были включены 94 пациентки с I–II стадиями РЯ и пограничными опухолями яичников, которые были рандомизированы в группу комплексной «активной» реабилитации (1-я группа, n=47) и группу «пассивной» реабилитации (2-я группа, n=47). Контрольную группу составили 80 женщин без онкогинекологических заболеваний. Программа комплексной «активной» реабилитации включала диету, нормированные физические нагрузки, коррекцию образа жизни, нутрициальную и медикаментозную поддержку. Оценка массы тела, индекса массы тела (ИМТ), объема талии (ОТ), объема бедер (ОБ), соотношения ОТ/ОБ проводилась до операции, через 1 нед, 1, 3, 6, 12, 24 и 36 мес.
Результаты. Исходно более 50% 1-й и 2-й групп пациенток имели избыточную массу тела или ожирение. Через 36 мес в 1-й группе зафиксировано значимое снижение массы тела и ИМТ (с 27,66±4,15 до 22,28±6,73 кг/м2; p=0,0362). Доля пациенток с нормальным ИМТ в 1-й группе увеличилась с 40,4% до 71,4%. Во 2-й группе, напротив, наблюдался рост ИМТ (с 26,90±2,62 до 27,81±3,06 кг/м2; p=0,0015) и уменьшение доли женщин с нормальным ИМТ до 16,7%. Значимые различия выявлены и в динамике соотношения ОТ/ОБ: в 1-й группе показатель снизился с 0,89±0,05 до 0,79±0,10 (p=0,0037), что указывает на переход из зоны «рискованного» в зону «хорошего» соотношения ОТ/ОБ и регресс абдоминального ожирения. Во 2-й группе соотношение ОТ/ОБ увеличилось до 0,96±0,07.
Заключение. Программа комплексной «активной» реабилитации демонстрирует высокую эффективность в коррекции массы тела и улучшении антропометрических показателей у пациенток после хирургического лечения ранних стадий РЯ. Долгосрочное применение мультимодального подхода позволяет не только снизить массу тела, но и добиться клинически значимого уменьшения абдоминального ожирения, в отличие от «пассивного» подхода к ведению таких пациенток в послеоперационном периоде, который ассоциирован с прогрессирующим увеличением веса и ухудшением антропометрических показателей.
Цель: обоснование включения входных параметров для нейронной сети, позволяющей осуществлять прогнозирование эффективности реабилитационных мероприятий с учетом утраты стойкой трудоспособности у больных туберкулезом легких.
Материал и методы. В исследование включены 335 пациентов с туберкулезом легких, из них 212 – с впервые выявленным заболеванием, 123 – с хроническими формами. Для прогнозирования эффективности реабилитационных мероприятий была разработана нейронная сеть на языке программирования Python 3.14. Архитектура сети базируется на многослойном персептроне с прямыми связями между нейронами и применением алгоритмов обратного распространения ошибки. В рамках данного исследования было признано целесообразным обеспечить прогнозирование утраты стойкой трудоспособности у пациентов с туберкулезом легких с помощью нейронной сети.
Результаты. В качестве входных параметров нейросети были интегрированы следующие: генотип DD гена GSTM1, генотип ЕЕ гена GSTT1, генотип ТС гена АВСВ1 и полиморфные варианты генов цитокинов – фактора некроза опухоли альфа (–308G>A (rs1800629)), интерлейкина (ИЛ) 1-бета (–31C>T (rs1143627)), ИЛ-4 (–589C>T (rs2243250)), ИЛ-10 (–592C>A (rs1800872)), ИЛ-10 (–1082A>G (rs1800896)), а также неблагоприятное рецидивирующее течение, множественная и широкая лекарственная устойчивость, сохранение дыхательной и легочно-сердечной недостаточности после курса реабилитации. Регрессионный анализ показал статистическую значимость всех входных параметров в отношении моделирования зависимой переменной. В результате тестирования нейронной сети точность прогноза («эффективность реабилитации») составила 88,3%.
Заключение. Применение нейронной сети для прогнозирования эффективности реабилитации пациентов с легочным туберкулезом обеспечивает высокую точность предсказания. Данный метод может быть внедрен в практическую деятельность врачей-фтизиатров для оценки степени развития стойкой утраты трудоспособности у таких больных. Предполагается, что представленная модель станет основой для комплексной программы реабилитации, охватывающей врачебные, профессиональные и социальные аспекты. ISSN 2949-5873 (print) ISSN 2949-5881 (online) Данная интернет-версия статьи была скачана с сайта https://rehabilitology.com. Не предназначено для использования в коммерческих целях. Инфор
ОБЗОРНЫЕ СТАТЬИ
Актуальность. Ишемический инсульт (ИИ) остается ведущей причиной инвалидизации взрослого населения. Эффективная реабилитация требует стандартизированных методов оценки исходов. Отсутствие согласия относительно набора объективных показателей осложняет интерпретацию данных и разработку клинических рекомендаций.
Цель: систематический анализ объективных методов контроля эффективности реабилитации пациентов с ИИ, оценка их валидности, воспроизводимости и практической применимости.
Материал и методы. Систематический поиск выполнен в соответствии с рекомендациями PRISMA 2020. Поиск публикаций с января 2000 г. по декабрь 2024 г. проводился в международных (PubMed/MEDLINE, Scopus, Web of Science, Cochrane Library, IEEE Xplore) и русскоязычных (eLibrary, КиберЛенинка) базах данных (последний поиск 15 декабря 2024 г.). В анализ включали исследования взрослых пациентов с ИИ, проходящих реабилитацию с использованием объективных методов оценки эффективности. Анализировали клинико-функциональные шкалы, нейровизуализационные, нейрофизиологические и биохимические биомаркеры, инструментальные биомеханические и цифровые методы. Оценку риска систематической ошибки проводили с применением инструментов RoB 2, ROBINS-I и QUADAS-2.
Результаты. На основании анализа ключевых систематических обзоров, консенсусных документов и репрезентативных первичных исследований систематизированы объективные методы контроля по шести категориям. Стандартизированные клинико-функциональные шкалы (шкала Фугл–Мейера, Шкала инсульта Национальных институтов здоровья США, индекс Бартела, Шкала функциональной независимости, тест для оценки функции руки, шкала баланса Берг) представляют наиболее валидированную основу для контроля эффективности реабилитации (качество доказательств умеренное – высокое). Инструментальные биомеханические методы обеспечивают высокую чувствительность к изменениям качества движений, но характеризуются высокой вариабельностью протоколов (качество доказательств низкое – умеренное). Нейровизуализационные, нейрофизиологические и биохимические биомаркеры демонстрируют значительный прогностический потенциал, однако остаются преимущественно исследовательскими инструментами (качество доказательств низкое – умеренное). Телереабилитационные и цифровые методы оценки создают возможности для объективного мониторинга в амбулаторных условиях (качество доказательств низкое).
Заключение. Оптимальный подход к контролю эффективности реабилитации у пациентов с ИИ предполагает использование стандартизированного набора клинических исходов как обязательного минимума с поэтапным добавлением инструментальных, нейрофизиологических и биомаркерных методов. Необходима дальнейшая разработка подходов к стандартизации объективных исходов в реабилитации данной когорты больных.
Эндопротезирование тазобедренного сустава во многих случаях является единственной возможностью для восстановления двигательной функции у пациентов с остеоартрозом, ревматоидным артритом, остеопорозом, а также после перелома проксимального отдела бедренной кости. Востребованность таких вмешательств с каждым годом увеличивается и в то же время сопровождается ростом числа послеоперационных осложнений. Многие из них (тромбоз глубоких вен, вывих, расшатывание эндопротеза) возникают вследствие недостаточного внимания к реабилитационным мероприятиям на до- и послеоперационном этапах. Лишь выполнение полного протокола лечебно-восстановительных мероприятий позволяет достичь максимальной функциональной эффективности сустава и обеспечить пациенту возвращение к привычной двигательной активности. В обзоре рассмотрены основные этапы реабилитации пациентов после эндопротезирования тазобедренного сустава – дооперационная реабилитация, обезболивание, ранняя послеоперационная реабилитация в условиях стационара и алгоритм амбулаторной реабилитации, включая коррекцию биомеханики походки. Комплексная реабилитация является обязательным условием для восстановления качества жизни после эндопротезирования тазобедренного сустава.
Развитие медицинской науки и здравоохранения позволяет существенно снизить риски прогрессирования тяжелых патологий печени у пациентов с метаболическими нарушениями. Неалкогольная жировая болезнь печени (НАЖБП) является глобальным вызовом для современной гепатологии и реабилитологии. Наиболее эффективный немедикаментозный метод, с помощью которого достигаются цели регресса стеатоза и улучшения метаболического профиля, – лечебная физическая культура (ЛФК). В обзоре проведен системный анализ эффективности различных режимов физических нагрузок в профилактике, лечении и реабилитации пациентов с НАЖБП. Рассмотрены биомеханические и молекулярные механизмы действия упражнений, обозначены современные техники дозирования аэробных и резистентных нагрузок, а также представлены возможности клинического применения ЛФК в составе комплексной терапии. Особое внимание уделено доказательной базе, основанной на данных рандомизированных контролируемых исследований и метаанализов.
С момента начала пандемии COVID-19 прошло уже более 5 лет, но вопросы реабилитации пациентов после перенесенной коронавирусной инфекции остаются актуальными. Так, в поисках новых методов реабилитации исследователи обратили внимание на интервальную гипокси-гипероксическую терапию (ИГГТ) как на средство восстановления утраченных физических и психологических резервов организма. Проведение ИГГТ способствует комплексной нормализации функций организма пациента путем воздействия на метаболические, иммунные процессы и антиоксидантную защиту. Многочисленные клинические исследования указывают на перспективность данного метода реабилитации, что подтверждается его эффективностью, безопасностью, сохранением достигнутого эффекта на протяжении 3–6 мес. Авторы рассмотренных в обзоре публикаций отмечают эффективность ИГГТ в лечении больных с сочетанной патологией. Однако ряд выявленных ограничений не позволяет масштабировать данный метод до стандартных протоколов реабилитации, что в совокупности с накопленными данными формирует запрос на проведение крупного многоцентрового исследования, в котором будет оценена эффективность и безопасность ИГГТ у пациентов с постковидным синдромом различных степеней тяжести.
Традиционные методы реабилитации часто имеют ограничения, связанные с недостаточной приверженностью пациентов, а также с отсутствием объективной обратной связи, необходимой для значительного улучшения функций. По этому необходимо использовать новые подходы для повышения мотивации больных и увеличения эффективности терапии. В этом могут помочь технологии виртуальной реальности (англ. virtual reality, VR) и дополненной реальности (англ. augmented reality, AR), которые все чаще используются в реабилитации. VR создает полностью иммерсивную цифровую среду, которая заменяет реальный мир, для чего требуется использование VR-очков. AR, напротив, накладывает цифровые элементы на реальную среду, позволяя пациентам видеть как свое физическое окружение, так и виртуальные подсказки с помощью смарт-очков, планшетов или VR-очков. Эта возможность обеспечивает обратную связь и поддержку в режиме реального времени в процессе выполнения упражнений. Показана эффективность применения VR- и AR-технологий в реабилитации пациентов с нарушениями функций организма, связанными с онкологическими заболеваниями, инсультом, рассеянным склерозом, черепно-мозговыми травмами, а также слабовидящих больных и людей с заболеваниями опорно-двигательного аппарата. Использование данных подходов приводит к уменьшению болевых ощущений, улучшению функциональных возможностей, психического здоровья и качества жизни. Продемонстрирована высокая приверженность больных к таким методам реабилитации. Рассмотрены причины успеха данных технологий, а также сложности, препятствующие их широкому внедрению в клиническую практику.
ISSN 2949-5881 (Online)