Перейти к:
Организация реабилитации при злокачественных новообразованиях репродуктивной системы
https://doi.org/10.17749/2949-5873/rehabil.2024.22
Аннотация
Актуальность. Достижения медицины позволили существенно увеличить продолжительность жизни пациенток с онкогинекологическими заболеваниями. На текущий момент одной из ключевых задач системы здравоохранения является восстановление и поддержание качества жизни онкологических больных, что актуализирует вопросы оптимизации системы реабилитации.
Цель: представить особенности организации реабилитационных мероприятий у пациенток с онкологическими заболеваниями гинекологического профиля.
Материал и методы. В обзор включено 75 публикаций на русском и английском языках, найденных в научных базах данных PubMed/MEDLINE, Google Scholar, ScienceDirect и онлайн-библиотеках eLibrary, КиберЛенинка, Cochrane Library, а также на сайтах научных сообществ и организаций. Отбор публикаций проведен с учетом рекомендаций PRISMA.
Результаты. Порядок оказания реабилитационной помощи пациенткам онкогинекологического профиля в отдельных аспектах схож с таковым при других онкологических заболеваниях. Показана эффективность нутритивной поддержки, лечебной физической культуры, физиотерапии и психологической помощи в восстановлении качества жизни и предотвращении развития осложнений. При проявлении дистресса, глубоких негативных психоэмоциональных нарушений, влияющих на физиологические процессы организма, хороший эффект оказывают йога, арт-терапия, когнитивно поведенческая терапия, гипнотерапия, трудотерапия и танцевально-двигательная терапия. Однако реабилитация у пациенток с онкологическими заболеваниями репродуктивных органов имеет ряд особенностей: необходимо проводить мониторинг состояния сексуальной функции и развития болевого синдрома, а также оказывать персонифицированную реабилитационную помощь. Данная специфика связана с изменениями гормонального фона, осложнениями после хирургического вмешательства и закрытостью пациенток при обсуждении вопросов сексуального здоровья.
Заключение. Реабилитация женщин после лечения онкогинекологических заболеваний восстанавливает утраченное благополучие, однако текущих мер поддержки недостаточно. Оказание комплексной персонифицированной реабилитации таким пациенткам в России не носит обязательного характера, что сказывается на длительности и эффективности восстановления здоровья женщин. Дальнейшее развитие реабилитационной помощи, в т.ч. через повсеместное внедрение комплексной реабилитации, позволит повысить ее качество и снизить финансовую нагрузку на систему здравоохранения.
Для цитирования:
Александров А.Г. Организация реабилитации при злокачественных новообразованиях репродуктивной системы. Реабилитология. 2024;2(2):247-263. https://doi.org/10.17749/2949-5873/rehabil.2024.22
For citation:
Aleksandrov A.G. Organization of rehabilitation for reproductive system malignant neoplasms. Journal of Medical Rehabilitation. 2024;2(2):247-263. (In Russ.) https://doi.org/10.17749/2949-5873/rehabil.2024.22
ВВЕДЕНИЕ / INTRODUCTION
В 2020 г. во всем мире было зарегистрировано 19,3 млн новых случаев злокачественных новообразований (ЗНО), из которых почти 10 млн привели к летальному исходу. Рак молочной железы стал наиболее часто диагностируемым ЗНО у женщин, обогнав даже рак легких. Из 2,3 млн выявленных новых случаев на рак молочной железы пришлось 11,7% всех диагнозов. За ним следует рак легких (11,4%), колоректальный рак (10%), рак простаты (7,3%) и рак желудка (5,6%). Рак шейки матки отмечен в 3,1% всех случаев онкологических заболеваний, а частота летальных исходов при нем составила 3,4%. На летальные исходы, ассоциированные с раком молочной железы приходилось 6,9% смертей [1].
Прогнозируется, что к 2040 г. глобальная заболеваемость опухолевыми патологиями дойдет до 28,4 млн случаев, что означает значительный рост – на 47% по сравнению с 2020 г. [1]. К 2070 г. распространенные виды ЗНО останутся примерно на тех же позициях по выявляемости. Ожидается увеличение частоты обнаружения колоректального рака на 2,9 млн случаев, рака молочной железы – на 2,3 млн, рака легких – на 1,7 млн, рака простаты – на 1,6 млн, рака желудка – на 0,3 млн, рака шейки матки – на 0,06 млн случаев. Данный прогноз указывает на глобальную тенденцию повышения заболеваемости раком, особенно в репродуктивной сфере. В последние десятилетия наблюдается заметный рост заболеваемости ЗНО у женщин репродуктивного возраста.
Распространенность онкологических заболеваний репродуктивных органов в России остается высокой, сопоставимой с мировой статистикой. По данным за 2021 г., на каждые 100 тыс. человек приходится 509,2 случая рака молочной железы, 191,6 случая рака тела матки, 126,7 случая рака шейки матки, 80,5 случая неоплазии яичников [2]. Эпидемиология опухолей в России и других странах демонстрирует значительный рост числа больных, обращающихся за медицинской помощью по поводу ЗНО, особенно онкопатологий, поражающих репродуктивную систему [3]. Они часто сталкиваются с проблемами, которые негативно влияют на качество жизни (КЖ) как из-за самого заболевания, так и из-за сложных диагностических и терапевтических процедур, послеоперационных осложнений и побочных эффектов химиотерапии. В результате пациентки могут испытывать ограничения в способности вести полноценную жизнь, а в некоторых случаях даже становятся инвалидами. Это может привести к ограничениям в реализации их профессиональных, социальных и личных интересов. Нередко женщины, больные раком, вынуждены увольняться с работы из-за снижения производительности труда, а их близким может потребоваться отпуск по болезни или внеплановый отпуск для ухода за ними в периоды обострения заболевания или после хирургических вмешательств.
Помимо физических последствий заболевания, крайне важно признать психологический аспект. Больные раком сильно подвержены эмоциональным нарушениям, стрессу, тревоге и депрессивным расстройствам. Им часто приходится сталкиваться с психологически травмирующими событиями, которые оказывают длительное влияние на все аспекты их жизни. Однако своевременная и комплексная реабилитация таких пациенток позволяет существенно снизить негативное воздействие на их физическое, психическое и эмоциональное благополучие [4].
Цель – представить особенности организации реабилитационных мероприятий у пациенток с онкологическими заболеваниями гинекологического профиля.
МАТЕРИАЛ И МЕТОДЫ / MATERIAL AND METHODS
Поиск публикаций / Search for publications
В обзор включены исследования, затрагивающие особенности организации реабилитации у пациенток с ЗНО репродуктивной системы. Для поиска были сформированы запросы на русском и английском языках: «реабилитация пациенток с раком репродуктивной системы», «реабилитация при раке в области гинекологии», «реабилитация онкогинекологических заболеваний», «организация реабилитации пациенток в гинекологии с раком», «особенности реабилитации пациенток в гинекологии с онкологией», «коррекция осложнения онкогинекологических заболеваний», “rehabilitation of patients with reproductive system cancer”, “rehabilitation for cancer in the field of gynecology”, “rehabilitation of oncogynecological diseases”, “organization of rehabilitation of patients in gynecology with cancer”, “features of rehabilitation of patients in gynecology with oncology”, “correction of complications of oncogynecological diseases”.
Поиск проведен в авторитетных научных базах данных PubMed/MEDLINE, Google Scholar и ScienceDirect, а также в онлайн-библиотеках eLibrary.ru, КиберЛенинка и Cochrane Library. В качестве дополнительных источников использованы сайты авторитетных научных сообществ и организаций, обнаруженные с помощью поисковых систем Яндекс и Google. Дальнейший отбор исследований выполнен с учетом рекомендаций PRISMA.
Отбор публикаций / Selection of publication
Поиск публикаций в представленных выше источниках по запросам на русском и английском языках позволил выявить 8757 публикаций. На этапе предварительного отбора определены 433 работы, затрагивающие тему обзора.
Далее была отсеяна 21 публикация по причине дублирования другой работы из альтернативного источника. Из 412 оставшихся публикаций только для 363 выявлены полнотекстовые версии, к которым был получен доступ. Подробное ознакомление с полными текстами для подтверждения релевантности работы, уникальности выводов и авторитетности источника показало, что лишь 75 публикаций полностью удовлетворяют критериям отбора.
Общая схема проведенного отбора публикаций в обзор приведена на рисунке 1.
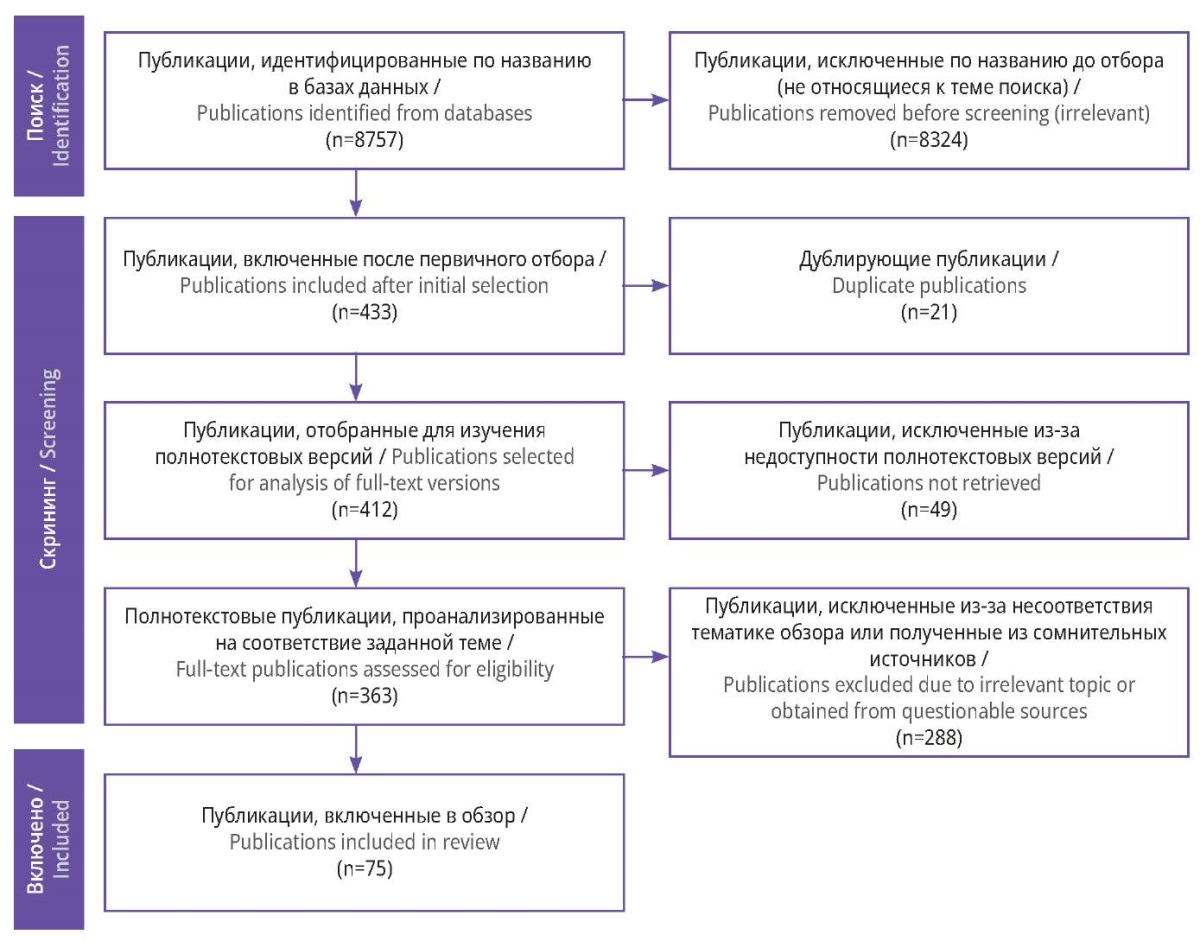
Рисунок 1. Блок-схема отбора публикаций с учетом рекомендаций PRISMA
(англ. Preferred Reporting Items for Systematic reviews and Meta-Analyses)
Figure 1. PRISMA (Preferred Reporting Items for Systematic reviews
and Meta-Analyses) workflow for selection of publications
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ / RESULTS AND DISCUSSION
Реабилитация онкогинекологических больных после противоопухолевой терапии / Rehabilitation of oncogynecologic patients after antitumor therapy
Специализированная противоопухолевая терапия играет решающую роль в лечении ЗНО, однако может привести к развитию различных осложнений, в т.ч. постовариэктомического синдрома (ПОЭС), дистресса, сексуальной дисфункции, болевого синдрома, общей интоксикации организма, синдрома хронической усталости, связанного с раком и его лечением. Каждое из этих осложнений требует конкретных корректирующих мер и стратегий восстановления [4].
Постовариэктомический синдром
Хотя развитие ПОЭС после лучевой терапии происходит медленнее и менее выражено, чем после хирургических вмешательств, у больных с экстрагенитальной патологией часто наблюдается тяжелое и затяжное течение данного осложнения. Следует отметить, что правосторонняя овариэктомия имеет тенденцию приводить к более заметным проявлениям синдрома по сравнению с левосторонней. Поэтому императивом становится рациональный подход к выбору адекватного хирургического лечения, по возможности отдающий предпочтение органосохраняющим операциям. Это поможет свести к минимуму осложнения, связанные с гипофункцией половых органов, гормональным дисбалансом и последующими физическими и психологическими проблемами, возникающими из-за гипоэстрогении, особенно у пациенток репродуктивного возраста [5][6].
ПОЭС, характеризующийся множеством клинических симптомов, возникает в результате внезапного прекращения функции яичников. Нейровегетативные и психоэмоциональные расстройства проявляются первыми, обычно в течение 24 ч после операции, и достигают пика примерно через 2–3 мес после завершения противоопухолевого лечения. В этот период постепенно возникают и усиливаются с течением времени метаболически-эндокринные, урогенитальные, сексуальные и другие нарушения. Женщины в возрасте от 30 до 40 лет особенно подвержены таким осложнениям в течение 0,5–2 лет после хирургического лечения.
Снижение уровня половых гормонов до следовых значений нарушает гормональный гомеостаз, повышает уровень холестерина в крови, изменяет липидный обмен, что подтверждается лабораторной диагностикой. Эти метаболические изменения могут впоследствии привести к развитию атеросклероза и/или ожирения. Кроме того, длительный дефицит эстрогенов негативно влияет на костную ткань, приводя к снижению уровней кальцитонина и паратгормона, что затрудняет всасывание кальция в костные структуры и способствует постепенному прогрессированию остеопороза. Поэтому крайне важно учитывать эти метаболические нарушения при разработке плана диеты для пациенток, проходящих противоопухолевую терапию, которую часто называют «противораковой диетой».
На этапе реабилитации после лечения рекомендуется принимать пищу не менее пяти раз в день, обеспечивая достаточную гидратацию. Кроме того, важно включать в рацион обогащенные продукты, богатые витаминами, минералами, незаменимыми аминокислотами и веществами с антиоксидантной активностью (клетчатка, фрукты, рыба, морепродукты, оливковое масло). Например, было обнаружено, что витамины С и Е повышают устойчивость клеток к повреждающим агентам, включая продукты распада опухоли и биотрансформацию лекарств. Однако некоторые ученые предостерегают от употребления чрезмерного количества антиоксидантов во время химиотерапии, поскольку это потенциально может затруднить разрушение злокачественных клеток и снизить эффективность лечения [7][8].
К счастью, существуют альтернативные решения этой проблемы. Соблюдение надлежащей гигиены половых органов и использование специальных смазочных гелей показали свою эффективность [9]. Эти средства повышают эластичность и упругость слизистой влагалища, способствуют регенерации тканей, устраняют сухость и зуд в области вульвы. Кроме того, доказана эффективность кремов и вагинальных суппозиториев, содержащих фитоэстрогены. Они снимают дискомфорт и раздражение в интимной зоне, оказывают противовоспалительное действие, уменьшают выраженность постлучевых осложнений, обеспечивают необходимую гидратацию, ускоряют процессы регенерации у молодых женщин [10].
Еще одним важнейшим аспектом реабилитации больных с ПОЭС является лечебная физкультура, желательно на свежем воздухе. Регулярные занятия активизируют обмен веществ и антиоксидантную систему, способствуя насыщению тканей кислородом, нормализации массы тела, уменьшению частоты приливов. Однако следует подчеркнуть необходимость наблюдения специалиста на этапах программирования и контроля начальных реабилитационных занятий, а также индивидуального подхода к каждой пациентке [11].
Кроме того, крайне важно, чтобы пациентки полностью воздерживались от курения и злоупотребления алкоголем. Эти факторы наряду с употреблением острой пищи усугубляют симптомы менопаузы, что может оказать негативное влияние на самочувствие женщины [12].
Дисбаланс гормонов также приводит к нарушениям микробиоты влагалища и колонизации патогенов [13]. Традиционно для решения этой проблемы использовались антибактериальные, антисептические и противогрибковые препараты. Однако сегодня все более распространенным становится применение пробиотиков, пребиотиков и синбиотиков для восстановления биотопа влагалища. Этот безопасный и эффективный метод направлен на мягкую иммуномодуляцию и снижение выраженности воспалительной реакции [14][15].
На текущий момент роль эстрогена широко изучена и доказано, что его дефицит способствует развитию урогенитальных расстройств. Эти нарушения характеризуются значительным снижением экспрессии рецепторов эстрогена и прогестерона в стенках влагалища. Однако коррекция данного состояния затруднена из-за многочисленных противопоказаний у онкологических больных гинекологического профиля к проведению как системной, так и местной гормональной терапии [16].
За последние несколько десятилетий достигнут значительный прогресс в области физиотерапии, позволивший нормализовать функции организма у пациенток с гинекологическим раком. Одной из конкретных областей, где физиотерапия показала многообещающие результаты, является коррекция ПОЭС. Положительные результаты наблюдались в центральной нервной системе пациенток за счет стабилизации функций мозга с помощью электросна, который имитирует физиологический сон, но имеет ряд преимуществ, таких как повышение насыщения крови кислородом и улучшение кровоснабжения мозга. Кроме того, обнаружено, что электросон повышает порог болевой чувствительности, усиливает реактивность сосудов и нормализует артериальное давление [17].
Для решения таких задач, как восстановление произвольного мочеиспускания и уменьшение отеков нижних конечностей, применяются электрическая стимуляция мочевого пузыря и пневматическая компрессия соответственно. Кроме того, ультразвуковая терапия, использующая механические колебания определенной частоты, позволяет усиливать кровообращение и оказывает противовоспалительный и обезболивающий эффект. Другой метод, применяемый с той же целью, – восходящий и круговой душ. За счет использования струй воды разного направления, давления и температуры улучшается микроциркуляция в тканях, что приводит к увеличению оксигенации [18]. Физические вмешательства, такие как электростатический и вакуумный массаж, также играют жизненно важную роль в расширении сосудов в целевых областях. Это, в свою очередь, приводит к увеличению скорости обменных процессов за счет улучшения кровоснабжения и притока кислорода. В конечном итоге все эти факторы способствуют восстановлению гомеостаза и улучшению общего функционирования организма [19].
Дистресс
Выявление онкологического заболевания может оказать глубокое и долговременное влияние на психическое благополучие женщины, особенно если заболевание диагностировано в молодом возрасте и поражает репродуктивные органы. Для людей, у которых диагностирован гинекологический рак, осознание диагноза и принятие его часто являются поворотным моментом, сопровождающимся дистрессом. Это негативная реакция организма на травмирующую ситуацию, характеризующаяся неприятными эмоциональными переживаниями, депрессией и тревогой. Она может нарушить поведение женщины, ухудшить ее психофизиологические функции, затруднить процесс выздоровления, снизить эффективность лечения, способствовать прогрессированию заболевания и значительно снизить общее КЖ [20].
Оказание психологической поддержки пациентке и ее семье становится одной из важнейших обязанностей лечащего врача. Для решения ряда проблем целесообразным становится участие психологов и психиатров в комплексных реабилитационных программах с целью нормализации психического состояния женщины, реализации персонализированного подхода и повышения эффективности клинического процесса.
Различные стадии заболевания, такие как дебют, рецидив, ремиссия и прогрессирование, требуют решения конкретных задач в зависимости от текущих жалоб пациентки, симптомов, отношения к своему состоянию и имеющихся ресурсов для адаптации. К психологической реабилитации онкогинекологических больных рекомендуется подходить через четыре организационных этапа, каждый из которых предполагает различные направления работы специалистов. На информационно-диагностическом этапе, совпадающем с подтверждением онкологии, основное внимание уделяется разъяснению алгоритма лечения. Психокоррекционный этап, который наступает на этапе госпитализации, сфокусирован на коррекции психологического развития и стратегии поведения, отклоняющихся от оптимальной модели. Психотерапевтический этап, начинающийся после хирургического вмешательства или в процессе химиотерапии, включает мероприятия, направленные на различные проблемы – эмоциональные, личные и социальные. Этап психореабилитации, направленный на восстановление и коррекцию нарушенных психических функций, является актуальным при чрезмерных психологических нагрузках у пациентки и при отсутствии оказания должной помощи на более ранних этапах [21].
Психологическое воздействие диагноза на больных гинекологическим раком является значительным и многогранным. Обеспечение адекватной психологической поддержки, применение персонализированных подходов и использование различных методов реабилитации могут значительно улучшить психическое благополучие и КЖ этих пациенток. Более того, на протяжении длительного процесса лечения женщины часто начинают испытывать повышенную тревогу, которая подпитывается страхом рецидива и побочных эффектов терапии. Экспериментальные данные показали, что у тревожных людей наблюдаются измененные реакции сердечно-сосудистой системы, такие как увеличение частоты сердечных сокращений, снижение вариабельности ритма в ответ на стресс и более медленное восстановление по сравнению со здоровыми людьми [22].
Танцевально-двигательная терапия – еще один эффективный подход к снижению тревоги и симптомов депрессии. Благодаря физической активности, связанной с танцами, высвобождается большое количество нейротрансмиттеров и нейротрофических факторов, действующих как естественные антидепрессанты. Танцевально-двигательная терапия сочетает в себе психологический компонент с мягкими физическими движениями, способствуя эмоциональной, физической и социальной интеграции [23].
Ресоциализация пациенток в профессиональном аспекте, например трудотерапия, также имеет решающее значение. Для многих женщин, особенно молодого возраста, возможность вернуться на работу тесно связана с успешной противоопухолевой терапией и общим КЖ. В тех случаях, когда возникают трудности или пациентка не решается вернуться к прежней работе, важно изучить альтернативные варианты трудоустройства, соответствующие ее навыкам и способностям. Полезно информирование больных о возможности переквалификации и приобретения новых навыков по профессиям, подходящим для их обстоятельств [24].
В последние годы получила распространение арт-терапия, которая использует творческую деятельность для облегчения исцеления. Ее можно проводить индивидуально или в группе. В реабилитации больных с онкогинекологической патологией групповая арт-терапия оказалась более эффективной, поскольку способствует взаимной поддержке женщин, уменьшению чувства одиночества и изоляции [25].
Также завоевал популярность такой терапевтический метод, как десенсибилизация и обработка движений глаз (англ. Eye Movement Desensitization and Reprocessing, EMDR). Эта методика фокусируется на адаптивной обработке информации и предполагает полифазный подход к решению различных аспектов травматического опыта, который можно проецировать на насущные проблемы пациенток онкогинекологического профиля [26].
В процессе реабилитации крайне важно выработать точное понимание болезни, охватывающее переживания, ощущения, эмоциональное состояние и отношения пациентки с окружающей средой. Исследования показали, что люди со склонностью к ипохондрии более подвержены нейровегетативным расстройствам. Для решения этих проблем часто рекомендуется когнитивно-поведенческая терапия, использующая изменение эмоциональных факторов и мыслей. Например, ведение дневника может помочь пациенткам ставить цели, записывать их и испытывать чувство удовлетворения от их достижения, что в конечном итоге улучшает общее состояние женщин. Основная цель когнитивно-поведенческой терапии – изменить внутреннее восприятие болезни, что приведет к повышению КЖ [22].
Йога – это практика, включающая серию упражнений, сочетающих медленные движения с укреплением мышц, что способствует улучшению физического и психического благополучия. Ее часто описывают как систематический способ достижения внутренней гармонии, а также гармонии с обществом и природой путем интеграции разума и тела в повседневную жизнь. Упражнения йоги не только увеличивают гибкость и силу мышц, но также облегчают боль и положительно влияют на физическую форму. Кроме того, доказано, что занятия йогой снижают кровяное давление и улучшают регуляцию обмена веществ. Сообщалось, что они повышают способность справляться со стрессом [27].
Таким образом, различные терапевтические подходы, такие как йога, когнитивно-поведенческая терапия, EMDR, арт-терапия, танцевально-двигательная терапия и трудотерапия, играют значительную роль в процессе реабилитации пациенток с онкогинекологической патологией. Они направлены на улучшение физического и психического благополучия, улучшение КЖ и содействие успешному возвращению к нормальной жизни как в личном, так и в профессиональном аспектах [28].
Нарушения сексуальной функции
Сексуальное здоровье играет важную роль в жизни большинства женщин. Однако в результате противоопухолевой терапии часто могут возникать сексуальные расстройства, которые вызывают личные и социальные трудности. Женская сексуальная дисфункция (ЖСД) включает такие симптомы, как боль, снижение сексуального интереса и удовлетворения. Данное осложнение при отсутствии должной поддержки приводит пациентку к ощущению непривлекательности, фригидности, низкой самооценке и ухудшению психологического благополучия. Многие женщины, страдающие от последствий проведенного лечения, также испытывают тяжелую диспареунию и дискомфорт из-за укорочения влагалища.
Некоторые исследования показали взаимосвязь между объемом хирургических вмешательств и возникновением ЖСД [29][30]. Эти проблемы обычно возникают примерно на 5-й неделе после противоопухолевого лечения и сохраняются в течение как минимум 6 мес после операции. Кроме того, лучевая терапия может усугубить ЖСД, приводящую к сухости, фиброзу, стенозу влагалища, сильной боли при минимальном прикосновении, посткоитальному кровотечению и даже неспособности поддерживать интимные отношения [31]. Сочетание хирургической и лучевой терапии связано с наиболее тяжелой формой ЖСД [32].
Заниматься решением сексуальных расстройств следует не только ради восстановления КЖ пациенток, но и потому, что нормализация сексуальной функции особенно важна для женщин репродуктивного возраста. Необходим комплексный подход, предполагающий решение анатомо-физиологических проблем и проведение психотерапевтических занятий под руководством квалифицированных специалистов. Также рекомендуется обратиться за консультацией к сексопатологу.
После хирургического лечения функциональные изменения в малых органах таза наряду с образованием спаек и развитием болевого синдрома существенно снижают сексуальную функцию и КЖ женщин. В тяжелых случаях это может даже привести к инвалидности. Поэтому профилактика послеоперационных осложнений имеет первостепенное значение. Персонализированные программы реабилитации, включающие контролируемые физические нагрузки, физиотерапию, дыхательную гимнастику, занятия в бассейне, минеральные воды, гало- и спелеотерапию, а также другие методы, доказали свою высокую эффективность. Однако важно, чтобы эти методы назначал специалист после тщательной консультации с учетом конкретного состояния пациентки [4].
Ароматерапия – безопасная процедура, которую можно использовать в качестве вспомогательного лечения ЖСД. Она способствует нормализации психического состояния, улучшению крово- и лимфообращения, гармонизации процессов в организме, тем самым повышая адаптогенность. На молодых женщин эфирные масла действуют как фитогормоны, стимулируя центры головного мозга и нормализуя психологическое и эмоциональное состояние. Наиболее эффективным методом коррекции ЖСД являются чередующиеся ингаляции эфирных масел лекарственных растений, оказывающих тонизирующее и расслабляющее действие на организм. Пациентки могут использовать отдельные масла или смеси. Рекомендуется пройти 2–3-недельный курс лечения с 20–30-минутными сеансами 2 раза в день, а впоследствии 2–3 дополнительных курса с интервалом 1–2 мес. После терапии женщины отмечают значительное улучшение самочувствия, включая снижение беспокойства, уменьшение приливов жара, снижение потоотделения и нормализацию артериального давления. Эти положительные изменения улучшают не только сексуальную функцию женщины, но и общее КЖ. Повторение курсов помогает закрепить достигнутые результаты [33].
Одним из частых осложнений хирургического лечения является лимфедема, которая отрицательно влияет на сексуальную функцию. Для решения этой проблемы традиционно используют магнитотерапию, позволяющую уменьшить выраженность нарушений микроциркуляции нижних конечностей [34]. Метод кинезиологического тейпирования, предполагающий наложение нейрофункциональных эластичных лент, также может использоваться для стимуляции нормального лимфотока и служить дополнительной терапией лимфедемы. Другие потенциальные варианты – ручной и аппаратный массаж, компрессионная терапия, электростимуляция, электрофорез и ультразвуковая терапия. Эти методы активизируют микроциркуляцию, способствуя восстановлению и регенерации в области лечения.
Лазерная терапия углекислым газом может использоваться для предотвращения стеноза влагалища и улучшения сексуальных реакций путем стимулирования изменений в коллагеновых и эластических волокнах. Женщины, испытывающие сухость слизистых оболочек, в качестве растворов могут использовать кремы, таблетки, кольца и другие средства. Кроме того, пациенткам может быть рекомендовано использование препаратов, содержащих гиалуроновую кислоту, для интимной контурной пластики, чтобы улучшить качество их сексуальной жизни [35].
Болевой синдром
Боль является часто встречающейся проблемой среди пациенток с гинекологическим раком. Важно различать острые и хронические болевые синдромы, причем основное различие заключается в качественном воздействии на организм, его нейрофизиологических и психофизиологических реакциях, а не только в продолжительности боли. Хронический болевой синдром существенно влияет на жизнь молодых женщин, приводя к снижению КЖ и представляя значимую медико-социальную проблему.
Чтобы не только облегчить боль после лечения онкогинекологических заболеваний, но и свести к минимуму возможные побочные эффекты, интересным методом оказалось применение терапевтических доз ксенона посредством ингаляций [36]. Ксенон бесцветен, не имеет запаха, негорюч и не биотрансформируется в печени, что делает его безопасным для использования. Исследования показали, что медицинский ксенон не обладает мутагенными, тератогенными, эмбриотоксическими и канцерогенными свойствами и не оказывает негативного влияния на репродуктивную систему [37]. В экспериментальных условиях больные гинекологическим раком, прошедшие ксеноновую терапию, сообщили о снижении артериального давления, сокращении интенсивности боли в различных областях, уменьшении раздражительности и улучшении качества сна [38].
Достижение эффективного облегчения боли является сложной и междисциплинарной задачей. В современной медицинской практике фармацевтические препараты играют решающую роль в лечении боли. На разных стадиях используются неопиоидные и опиоидные анальгетики, а также вспомогательные и симптоматические средства, такие как противосудорожные препараты, антидепрессанты, спазмолитики, снотворные и глюкокортикостероиды [39].
В качестве дополнительного метода можно рекомендовать гипнотерапию. Используя силу разума и мышления, гипнотерапия помогает пациенткам отвлечься от болевых ощущений. Недавние исследования показали, что дистанционная гипнотерапия, проводимая посредством видеосвязи или интернета, менее эффективна по сравнению с личным общением пациентки и врача [40][41]. Однако эта форма реабилитации может быть доступной для всех женщин, в т.ч. для тех, кто проживает в отдаленных районах и не имеет свободного доступа к реабилитационным центрам.
Интоксикация организма
В процессе реабилитации крайне важно уделять внимание детоксикации организма. Для достижения этой цели больным гинекологической онкологией может быть проведена эфферентная терапия, которая включает различные методики, позволяющие смягчить негативные последствия лечения, и помогает вывести из организма ряд веществ, в т.ч. эндогенные и экзогенные токсины, чужеродные белки, химические соединения, патологические продукты и агрессивные ферменты.
Широко используемым методом эфферентной терапии является гемосорбция. Этот метод направлен на удаление различных токсинов из сосудистого русла с помощью специального сорбента, способного связывать с его поверхностью опасные молекулы – как правило, за счет заряда или свободного радикала. Общим показанием к данному виду лечения является тяжелая эндогенная интоксикация, подтвержденная клиническими и лабораторными исследованиями. Лечебный эффект гемосорбции включает устранение избытка синтезируемых метаболитов, улучшение периферического кровообращения и реологических свойств крови, коррекцию симптомов кислородной недостаточности, уменьшение площади ишемических зон в органах и тканях.
Одним из методов детоксикации является плазмаферез, который предполагает удаление из кровотока продуктов метаболизма и излишков лекарственных веществ. Этот терапевтический подход использует несколько механизмов: устранение чужеродных веществ из микровенозной системы, усиление функционирования кроветворных и иммунокомпетентных клеток, улучшение кровообращения. Удаленную плазму заменяют специальными растворами – коллоидами или кристаллоидами. К положительным эффектам плазмафереза относятся снижение артериального давления, уменьшение мышечных, суставных и головных болей, регуляция секреции потовых желез, улучшение психоэмоционального состояния, существенное повышение качества сна [42][43].
Синдром хронической усталости
Усталость, которую испытывают онкологические больные, сильно отличается от усталости у здоровых людей. Она выходит за рамки простого чувства утомления и может оказать существенное влияние на повседневную жизнь пациенток. Они сталкиваются с трудностями при выполнении простых задач, попытках концентрации внимания и при принятии решений, а также с проблемами потери памяти и нарушения режима сна. Могут присутствовать физические симптомы, такие как одышка, головокружение и повышенная эмоциональная чувствительность, сексуальная дисфункция и ощущение полной слабости. Это особенно беспокоит молодых пациенток, поскольку нарушает их активный образ жизни и значительно снижает общее КЖ [44].
Для решения данной проблемы признаны полезными дополнительные адъювантные и альтернативные методы лечения. Медитация, музыкальная терапия, иглоукалывание, массаж, йога, фитотерапия и электростимуляция показали многообещающие результаты в снижении усталости и улучшении самочувствия женщин с гинекологическим раком. Исследования показали, что эти подходы способны уменьшить тревогу и депрессию и повысить общее КЖ таких пациенток [45].
Выбор вариантов лечения и индивидуальных программ зависит от различных факторов, в т.ч. от наличия других заболеваний, продолжительности пребывания в санатории и собственного настроения пациентки. Кроме того, для больных крайне важно иметь систему поддержки и возможность общаться с другими людьми, переживающими аналогичный опыт. Это позволяет им получать советы от людей, которые понимают их ситуацию.
Одним из особенно эффективных методов электростимуляции является чрескожная электрическая нейростимуляция. Исследование, проведенное в больнице Шэньси в Китае с декабря 2015 г. по ноябрь 2017 г., подтвердило эффективность данного подхода. Показано его положительное влияние на больных, проходящих лечение по поводу гинекологической онкологии, особенно при сочетании с санаторно-курортным лечением в периоды ремиссии. Санаторно-курортное лечение предполагает воздействие на пациенток природных факторов, таких как климатические условия, воздушные ванны и водные источники, для укрепления собственных защитных механизмов организма и восстановления нарушенных функций [46].
Реабилитация – задача здравоохранения XXI века / Rehabilitation is а challenge for healthcare in the 21st century
В связи с существенным прогрессом в медицине и увеличением продолжительности жизни пациентов в XXI веке реабилитация стала основной стратегией общественного здравоохранения, которое сегодня фокусируется не только на снижении смертности, но и на улучшении функционирования и КЖ человека. Международные эксперты считают, что реабилитация является ключом к оптимизации способности человека выполнять привычные действия – как физиологические, так и социальные. Основная цель реабилитационных мер − предотвратить или свести к минимуму ограничения функционирования (подвижность, когнитивные функции, дыхание, зрение и общение). Всемирная организация здравоохранения (ВОЗ) подчеркивает необходимость расширения доступа к реабилитационным программам, особенно при неотложной и травматологической медицинской помощи [47].
Интеграция реабилитации в систему здравоохранения и обеспечение раннего доступа к услугам могут привести к оптимальным результатам медицинских вмешательств и снизить риск осложнений и ограничений. Это, в свою очередь, улучшает общее состояние здоровья и КЖ пациентов, одновременно снижая экономическую и социальную нагрузку на систему здравоохранения [4][48]. Подход ВОЗ к реабилитации делает акцент на комплексном уходе за отдельными людьми, а не на конкретных заболеваниях. Его целью является устранение ограничений в функционировании на протяжении всего периода оказания медицинской помощи и в течение всей жизни человека. По мере того как страны переходят к личностно-ориентированному лечению, крайне важно включать высококачественную реабилитацию в модели предоставления услуг.
Реабилитация все чаще признается долгосрочной моделью ухода, которая способствует восстановлению утраченных функций и улучшает КЖ пациентов. Своевременная реабилитация не только приносит пользу больному и его близким, но также оказывает положительное влияние на здравоохранение и другие сектора, такие как социальные услуги, образование и труд. Это снижает количество госпитализаций, повторных госпитализаций, дорогостоящих осложнений, а следовательно, общую экономическую нагрузку на систему здравоохранения и государство. Человек, который восстанавливает функционирование посредством реабилитации, вновь обретает независимость, возобновляет образование и трудовую деятельность, а также снижает свою потребность в постоянном уходе и поддержке со стороны социальных служб или семьи [49].
Профилактика рецидивов в реабилитационном периоде / Prevention of relapses during rehabilitation period
Проведение противорецидивных мероприятий – важнейшая составляющая процесса реабилитации при любом виде рака. После завершения лечения пациентам важно продолжать постоянное медицинское наблюдение. Одним из потенциальных решений для предотвращения прогрессирования заболевания является использование поддерживающей терапии, которая включает соблюдение определенного режима дня, обеспечивающего достаточно времени для сна и отдыха, а также индивидуальной противораковой диеты.
Кроме того, больные проходят диагностический мониторинг сывороточных маркеров для выявления любых аномальных показателей. Если наблюдаются значительные изменения, может быть рекомендовано применение методов визуализации, таких как ультразвуковое исследование, магнитно-резонансная томография и компьютерная томография [50]. Необходимо разъяснять важность регулярных посещений врача и соблюдения всех назначенных методов лечения в соответствии с клиническими рекомендациями.
В последние годы все больше внимания уделяется роли нутриентов в лечении рака. Клинические и эпидемиологические данные показали корреляцию между низкими концентрациями витамина D в организме пациентов и ростом распространенности ЗНО. Более высокий уровень потребления витамина D может оказывать защитное действие против рака яичников и молочной железы. И наоборот, низкий уровень витамина D связан с повышенным риском развития рака. Кроме того, по результатам исследований, более высокие уровни витамина D связаны со снижением агрессивности рака [51][52]. Метаанализ десяти клинических исследований с участием более 80 тыс. человек продемонстрировал, что у больных раком, принимавших препараты витамина D, наблюдался более низкий уровень смертности [53].
Исследования показали, что развитие рака связано с нарушениями в работе иммунной системы и иммунобиологического надзора. Таким образом, иммунотерапия стала перспективным подходом. Иммунотерапию можно разделить на четыре типа:
- активная иммунотерапия, предполагающая использование цитокинов, бактериальных препаратов и вакцин;
- пассивная иммунотерапия, в которой применяются моноклональные антитела;
- специфическая иммунотерапия с использованием специфических антигенов или антител;
- неспецифическая иммунотерапия.
В целом этот метод лечения направлен на подавление прогрессирования опухоли и стимуляцию иммунного ответа, что приводит к подавлению злокачественного роста, элиминации опухолевых клеток и снижению риска рецидива за счет развития иммунологической памяти [54].
Принципы организации реабилитации / Principles of organizing rehabilitation
По мнению H. Hoenig et al., для успешной реализации стратегии реабилитации крайне важно понять основные факторы, которые способствуют ограничениям функционирования или инвалидности в каждом конкретном случае. После выявления этих факторов можно выстроить индивидуальный диагностический подход и выбрать соответствующую тактику лечения [55].
Существует две традиционные концептуальные модели, используемые для ведения пациентов с ограниченными возможностями: биомедицинская и биопсихосоциальная. Характер и тяжесть инвалидности во многом определяются взаимодействием человека с его социальной и экологической средой, а также способностью общества сосуществовать и заниматься совместной деятельностью с людьми, частично утратившими полноценное функционирование. Лечение этой категории лиц в основном зависит от внешних факторов, влияющих на разные стадии развития нарушений в конкретной системе органов. Например, своевременное и правильное лечение заболевания может предотвратить утрату определенных функций, а реабилитационная помощь – помочь восстановить частично утраченные функции и улучшить КЖ. Предоставление вспомогательных устройств также помогает интегрировать пациентов в общество и позволяет им заниматься своей обычной деятельностью, которая без специального оборудования была бы недоступна [56].
Принципы организации реабилитации должны быть основаны на своевременном оказании специализированной помощи и преследовать цель разорвать цикл взаимодействия внутренних и внешних факторов, способствующих формированию и прогрессированию патологии. Пол, возраст и раса связаны с различиями в риске инвалидности, хотя точный их вклад до конца не изучен [57]. Это может быть обусловлено различиями в вероятности возникновения сопутствующих заболеваний и расстройств, продолжительности жизни, доступе к профилактическому медицинскому обслуживанию, социально-экономическом статусе, а также с культурными и образовательными различиями, которые влияют на то, как люди справляются с нарушениями и инвалидностью.
Существуют факторы, способные изменить риск инвалидности. Они могут быть внутренними (эндогенными) или внешними (экзогенными). Внутренние факторы включают психологические аспекты, такие как мотивация и депрессия, а также образование, культура и связанные с ними заболевания, которые повышают риск инвалидности. Петли обратной связи между различными расстройствами также способствуют прогрессированию инвалидности. Например, нарушение походки может вызвать падение пациента и повреждение конечности, что приведет к новым дефектам и функциональным ограничениям. Внешние факторы включают медицинские вмешательства, такие как профилактические меры, лекарства, хирургические процедуры и реабилитация, а также социальную поддержку и финансовые аспекты [58].
Биомедицинская модель ориентирована на изучение причин и последствий патологических процессов в живых организмах. В первую очередь рассматриваются этиология и патофизиология заболеваний, прослеживаются причинно-следственные связи. Эта модель более применима к линейным и однонаправленным процессам. С другой стороны, биопсихосоциальная модель учитывает среду, в которой развилось заболевание, а также внешние факторы, способствовавшие его формированию. Также принимается во внимание влияние этих факторов на функционирование и благополучие пациента в обществе.
Инвалидность рассматривается как совокупность биологических, анатомических и физиологических нарушений, социальной дезадаптации и экономических потерь. Поэтому логичным подходом к снижению инвалидности является использование комбинации обеих моделей. ВОЗ приняла концептуальную основу, отражающую поэтапный процесс от триггеров заболевания до исхода инвалидности, принимая во внимание все сопутствующие события, которые способствуют прогрессированию заболевания [59].
Подходы к реабилитации онкогинекологических больных / Approaches to rehabilitation of oncogynecologic patients
Значительные успехи в диагностике опухолей и внедрении новых высокотехнологичных методов лечения заметно улучшили продолжительность жизни и 5-летнюю выживаемость онкологических больных [60]. Однако хирургические вмешательства по-прежнему могут быть агрессивными, а такие методы лечения, как лучевая терапия, химиотерапия и заместительная гормональная терапия, часто сопровождаются различными побочными эффектами.
В некоторых случаях эти методы лечения могут привести к тяжелым состояниям, вызванным неспособностью организма адаптироваться. У больных гинекологическим раком, в частности, может возникнуть хирургическая менопауза и развиться мочеполовой менопаузальный синдром, который включает такие симптомы, как вульвовагинальная атрофия, диспареуния, дизурия, рецидивирующие урогенитальные инфекции, сексуальная дисфункция и психологические проблемы. Эти последствия могут быть особенно тяжелыми для пациенток репродуктивного возраста, которые все еще желают иметь семью. В результате женщины часто с трудом справляются со своими обстоятельствами и могут замкнуться в обществе, испытывая апатию и дезадаптацию. Поэтому важно не только сосредоточиться на клиническом выздоровлении пациентки, но и помочь ей восстановить чувство нормальности, способность реинтегрироваться в общество [61].
Хотя реабилитация обычно проводится в условиях больницы для восстановления и оптимизации функциональных возможностей, важно также учитывать физические нарушения, которые могут возникнуть во время лечения рака. Раннее распознавание этих нарушений имеет решающее значение для скорейшего начала процесса выздоровления не только в реабилитационном отделении, но и во время лечения пациентки у онколога. Онкологи и специалисты реабилитационной медицины должны совместно разработать и реализовать индивидуальную программу реабилитации для каждой пациентки с учетом стадии заболевания, этапа лечения и уровня нарушений.
Когда у женщины диагностируют рак репродуктивной системы, комплексный подход с привлечением команды различных специалистов необходим на каждом этапе пути пациентки – начиная с момента постановки диагноза, на протяжении всего процесса лечения и даже в период ремиссии. Важно не только оценить физическое состояние больной, но и ее психологическое состояние и оказать необходимую поддержку. По мнению S.L. Anwar et al., программы реабилитации онкологических больных направлены на улучшение КЖ и помощь в достижении независимости и самоопределения. Это становится возможным благодаря команде врачей разных специальностей, в т.ч. онкологов, акушеров-гинекологов, врачей-реабилитологов, психологов, физиотерапевтов, логопедов, специалистов по реабилитационному сестринскому делу [62].
Чтобы обосновать необходимость реабилитационных мер, следует сформулировать четкие цели и конечные результаты. Обычно план реабилитационной терапии включает сохранение трудоспособности пациенток и обеспечение благоприятного прогноза, адаптацию к перестройке функционирования организма в случаях снижения или утраты трудоспособности, оказание паллиативной помощи больным с опухолями на поздних стадиях. Реабилитация пациенток с гинекологическим раком требует поэтапного, непрерывного и последовательного подхода, который начинается как можно раньше. Она должна быть адаптирована к индивидуальным потребностям женщин и иметь социальную направленность. Необходимо обеспечить активное участие пациентки и ее семьи в процессе выздоровления, а также междисциплинарный подход [63].
В последнее время в литературе заметно чаще стали использовать термин «пререабилитация». Под ним подразумеваются реабилитационные мероприятия, которые проводятся между постановкой диагноза и началом лечения. Причина такого повышенного внимания к предварительной реабилитации состоит в том, что именно в этот период пациентки наиболее уязвимы к развитию психических расстройств и реактивных состояний, требующих профессиональной помощи. В целом концепция пререабилитации получила признание в медицинском сообществе. Необходимы дальнейшие исследования и комплексные программы для решения физических, пищевых и психологических аспектов пререабилитации, чтобы обеспечить пациенткам наилучший уход. В течение этого периода специалисты стремятся предотвратить потенциально травматическое воздействие самого диагноза. Их цель – помочь женщине смириться с текущей ситуацией и найти потенциальные решения своей проблемы. Это раннее вмешательство имеет большое значение для обеспечения благоприятного результата всего плана лечения [64].
E. Miralpeix et al. предложили мультимодальную программу предварительной реабилитации при онкогинекологических заболеваниях, направленную на оптимизацию терапии с включением физических упражнений, консультирования по вопросам питания и оказания психологической поддержки. Авторы делают акцент на целесообразности проведения пререабилитации перед плановой операцией по поводу гинекологической онкологии [65].
В проспективном многоцентровом исследовании, проведенном А. Vonk Noordegraaf et al., участвовали 215 пациенток, перенесших гистерэктомию или лапароскопическую операцию по поводу доброкачественных образований придатков. Женщины получили персональные рекомендации по повседневной деятельности, работе и саморазвитию до и после операции. Результаты показали, что комплексная программа реабилитации с пререабилитацией eHealth оказала значительное положительное влияние на скорость возвращения пациенток к работе, снижение интенсивности боли и общее КЖ. К сожалению, авторы не предоставили подробной информации о физическом, нутритивном и психологическом статусе больных [66].
Согласно программе ускоренного восстановления после операции (англ. Enhanced Recovery After Surgery, ERAS), которая с 2014 г. является стандартным хирургическим подходом для данной категории пациенток, женщины старше 18 лет, перенесшие плановые гинекологические онкологические процедуры, имеют право на консультацию хирурга и анестезиолога в рамках пререабилитационной программы. Пациентки должны подписать информированное согласие во время предварительного обследования. После официального включения в программу все женщины проходят три оценочных визита: во время постановки диагноза (исходный уровень), за 1 нед до операции и через 8 нед после операции. Первичная оценка проводится примерно за 2–4 нед до назначенной даты хирургического вмешательства во время предоперационной инструментальной диагностики (компьютерная томография или магнитно-резонансная томография). На исходном этапе определяют предоперационный статус с учетом пищевых, физических и психологических факторов, а также результатов скрининговых исследований. На основании этой оценки пациенткам назначают программу либо на дому, либо под профессиональным наблюдением. За 1 нед до операции (предоперационный этап) и через 8 нед после нее (послеоперационный период) оценивают соответствие физиологических и психологических показателей в ежедневных записях пациенток, а затем повторно определяют их физическое, пищевое и эмоциональное состояние. После хируригической процедуры женщины проходят мультимодальную реабилитацию как во время пребывания в стационаре, так и после выписки, в общей сложности в течение 8 нед. Помимо специализированных консультаций всем им предоставляется информационный буклет, содержащий инструкции по физической активности, пищевым добавкам и методам релаксации. В него также включен дневник, в котором пациентки должны документировать свои действия. Хотя рекомендуемая длительность пререабилитации составляет 2–4 нед до операции, реальная продолжительность программы не фиксирована и зависит от состояния пациентки, типа опухоли и ее распространенности.
Женщины с раком репродуктивной системы представляют собой разнородную группу с различными заболеваниями, поэтому реабилитационные мероприятия адаптируются и персонализируются в зависимости от их функционального состояния, сопутствующих заболеваний и типа опухоли. Например, у пациенток с раком эндометрия и шейки матки рекомендуемая продолжительность предварительной программы реабилитации составляет 2–4 нед, охватывая период между диагностикой и операцией, в течение которого больные проходят дополнительную предоперационную диагностику с использованием расширенных инструментальных и лабораторных исследований. При раке яичников все пациентки начинают предварительную реабилитацию на стадии подозрения на рак или во время диагностики, а продолжительность программы варьируется в зависимости от выбранного подхода к лечению. В случаях первичной операции по удалению опухоли между стандартными анализами и исследованиями, как правило, назначается 2-недельный период пререабилитации, в течение которого с помощью лапароскопического диагностического вмешательства и первичной операции устанавливают степень и стадию заболевания. В случаях «интервальной» операции по удалению опухоли больные проходят пререабилитацию во время неоадъювантной химиотерапии, которая обычно длится 2 мес [65][67][68].
В ходе непрерывного и широкомасштабного исследования с участием нескольких центров A.L. Hawkes et al. провели клиническое исследование фазы II, посвященное стратегиям снижения веса у пациенток с ожирением и ранней стадией рака эндометрия. В него были включены три группы больных, получавших гормональное лечение с применением внутриматочной спирали, содержащей левоноргестрел, с добавлением метформина или без него. Исследователи полагают, что такой комплексный подход, сочетающий меры по снижению веса с гормональным лечением, может принести пользу пациенткам с раком эндометрия за счет уменьшения потребности в госпитализации и побочных эффектов, связанных со стандартным лечением, тем самым снижая затраты на здравоохранение [69].
В настоящее время реабилитационные центры многих стран Европы предлагают санаторно-курортные программы, включающие наиболее эффективные физиотерапевтические методы восстановления онкогинекологических больных: пневматическую компрессию, электрическую стимуляцию мышц, магнитотерапию, лечебный массаж и упражнения в бассейне. Кроме того, эти центры предоставляют комплексную помощь высококвалифицированных врачей, специализирующихся как на онкологических заболеваниях, так и на реабилитации. Используются различные реабилитационные программы, такие как аэротерапия, климатотерапия, ландшафтная терапия, лечебное питание, лечение минеральными водами. Психологическая поддержка также является важным аспектом такого лечения: как групповая, так и индивидуальная психотерапия, а также когнитивно-поведенческая терапия, арт-терапия, медитация и трудотерапия применяются для поддержания психологического благополучия онкологических больных [70].
После завершения специфической терапии начинается этап реабилитации. Основными ее задачами являются предотвращение послеоперационных осложнений, восстановление нарушенных функций (например, мышц таза), устранение любых расстройств, возникших во время лечения (например, мочеполового климактерического синдрома), а также улучшение общего КЖ пациентки, включая сексуальное здоровье и способность активно участвовать в жизни общества. Конечная цель – оптимизировать или восстановить физическую, психосоциальную и профессиональную деятельность женщины до предракового уровня. Для пациенток со значительными функциональными нарушениями реабилитация направлена на их способность выполнять задачи по самообслуживанию и мобильности, включая обучение использованию протезов и инвалидных колясок, а также эмоциональную поддержку и адаптацию к нарушениям. Для больных с запущенным раком программы паллиативной реабилитации предназначены для обеспечения комфорта и самопринятия посредством обезболивания, профилактики пролежней и психологической поддержки. После предварительной реабилитации проводится последующий процесс специфической терапии, адаптированный к конкретному диагнозу в области гинекологической онкологии. Данная терапия включает ряд методов лечения, таких как хирургия, химиотерапия, лучевая терапия и заместительная гормональная терапия. Крайне важно в этот период не только придерживаться современных рекомендаций по лечению, но и информировать пациентку о возможных побочных эффектах, регулярно следя за их развитием, оказывать симптоматическую поддержку, а также направлять к психологам и психотерапевтам для поддержания психологического благополучия [63].
В ходе ретроспективного анализа, проведенного C. Falcicchio et al. [71], изучена региональная база данных системы здравоохранения административной области Лацио (Италия), в которой особое внимание уделялось 5538 женщинам c диагностированным раком молочной железы. Большинство пациенток (81,7%) получали амбулаторную реабилитационную помощь, которая в первую очередь была направлена на само заболевание с гораздо меньшим упором на восстановление утраченных функций в результате заболевания и его лечения, таких как двигательная реабилитация и психологическая поддержка. Примечательно, что лишь небольшое количество женщин (1,3%) участвовали в стационарных программах, и еще меньшее (1%) – в интенсивной амбулаторной реабилитации. Авторы пришли к выводу, что значительная часть пациенток не получает адекватной реабилитационной помощи в течение 1-го года после постановки диагноза [71].
Таким образом, необходимо предоставлять пациенткам более полную информацию о различных доступных им методах реабилитации, а также совершенствовать структуру существующих реабилитационных программ. Это обеспечит женщинам с опухолями репродуктивной системы доступ к полному набору реабилитационных мер. Для детальной разработки стратегических программ реабилитации необходимы дальнейшие исследования.
Неудовлетворенные потребности пациентов / Unmet patient needs
Во многих странах отсутствие комплексной программы реабилитации в системе здравоохранения привело к неудовлетворению потребностей пациентов.
В ходе опроса, проведенного L. Thorsen et al. [72] в Норвегии в 2008 г., выполнена оценка потребности в реабилитации у больных, страдающих наиболее распространенными типами рака. Результаты показали, что большинство респондентов либо нуждались в дополнительных реабилитационных услугах, либо считали полученные услуги неадекватными. В опросе приняли участие 1325 человек, женщины составили 70% выборки, средний возраст респондентов – 52 года. Из опрошенных 63% заявили о необходимости хотя бы одной формы реабилитации. Чаще всего сообщалось о потребностях в физиотерапии (43%), лечебной физкультуре (34%), психологическом консультировании (27%) и многопрофильных групповых упражнениях (24%). Другие упомянутые потребности включали специализированные реабилитационные центры и санатории (24%), консультации социальных работников (19%) и эрготерапевтов (6%). Те, у кого произошли изменения в статусе занятости из-за болезни или химиотерапии, сообщили о более высоком спросе на комплексные программы реабилитации. Примерно 40% участников выразили недовольство имеющимися услугами [72].
В исследовании P.N. Butow et al. [73] проведен анализ КЖ и неудовлетворенных потребностей лиц, осуществляющих уход за женщинами с раком яичников на последнем году их жизни. Исследователи обнаружили, что у людей, занимающихся уходом, более низкое КЖ, пониженные оптимизм и социальная поддержка, более высокий уровень психологического стресса и неудовлетворенные потребности в психосоциальной реабилитации по сравнению с населением в целом. Эти переживания были в первую очередь связаны с прогнозом больной, страхом перед прогрессированием опухоли, хрупким балансом между их собственными потребностями и потребностями пациентки, влиянием обязанностей по уходу на их работу и принятием решений в неопределенных условиях. Авторы пришли к заключению, что лица, осуществляющие уход за пациентками с гинекологической онкологией, также нуждаются в помощи для решения эмоциональных проблем, связанных с их моральными обязанностями [73].
M. Seland et al. [74] показали, что женщины, проходящие лечение от рака репродуктивной системы, испытывают значительные страдания. В исследование были включены 92 пациентки, которые за последние 2 года проходили терапию онкогинекологических заболеваний. Среднее время с момента окончания лечения составило 7,6 мес с диапазоном от 0 до 24,5 мес. В общей сложности 57% участниц отметили дистресс, при этом усталость (58%), покалывание в руках или ногах (54%), беспокойство (53%) и проблемы с памятью/концентрацией (50%) были наиболее частыми жалобами. Проблемы охватывали различные области, такие как отношения с партнерами, эмоциональные расстройства (например, депрессия, страхи, нервозность, грусть, тревога и потеря интереса к обычной деятельности), внешний вид, память/концентрация, боль, сексуальные отношения, сон и снижение физической выносливости. Значительная часть (52%) женщин сообщили о неудовлетворенных потребностях в реабилитационных услугах. Распространенность дистресса среди пациенток, получающих лечение по поводу гинекологического рака, оказалась высокой, причем с ним связано множество проблем и неудовлетворенные потребности в реабилитационных услугах [74].
В комплексном исследовании, проведенном L.V. Holm et al. [75], изучено влияние сопутствующих заболеваний на необходимость реабилитационных программ для людей с раковым анамнезом. Это популяционное когортное исследование длилось 14 мес с момента постановки диагноза и включало пациентов из двух регионов Дании. Через 14 мес после постановки диагноза участники прошли анкетирование для получения мнения о различных аспектах их жизни, включая потребность в реабилитации и участие в реабилитационных мероприятиях. Результаты выявили значительную связь между наличием сопутствующих заболеваний и необходимостью проведения физической реабилитации. Более того, наличие сопутствующих патологий от умеренной до тяжелой степени соотносилось с более широким спектром потребностей при оказании помощи на восстановительном этапе. Эту информацию следует учитывать при разработке стратегий оказания реабилитационной помощи пациентам, страдающим онкологическими заболеваниями, в т.ч. и гинекологического профиля [75].
Опираясь на существующую литературу, можно сделать вывод, что значительная доля пациентов остается неудовлетворенной объемом и эффективностью проводимой реабилитации. Это подчеркивает необходимость тщательного планирования программ восстановления, своевременной их реализации в процессе лечения и сострадательного подхода к больным. Такие усилия помогут выявить потенциальное снижение КЖ или нарушения адаптивных ресурсов.
ЗАКЛЮЧЕНИЕ / CONCLUSION
Реабилитация играет решающую роль в восстановлении благополучия женщин с онкологическими заболеваниями, затрагивающими репродуктивную систему. В то время как многие западные страны успешно интегрировали систему комплексной реабилитации в лечение онкологических больных гинекологического профиля, в России такая система находится еще в ранней фазе своего становления. Это связано как со сложностью ведения пациенток на восстановительном этапе, так и с общими проблемами в системе реабилитации (нехватка медицинских учреждений, образовательных инициатив и государственного финансирования), которые препятствуют предоставлению адекватных реабилитационных услуг.
При этом существуют доказательства экономической эффективности оказания восстановительной помощи, связанной с сокращением затрат на дальнейшую медицинскую поддержку для коррекции осложнений, рецидивов, психосоциальных проблем, снижением частоты и длительности госпитализаций. Реабилитационные мероприятия у женщин с онкогинекологическими заболеваниями помогают устранять функциональные ограничения и потерю профессиональной активности.
Для разработки комплексной концепции реабилитации в России необходимы дальнейшие исследования, включая экономическую оценку эффективности медицинских технологий.
Список литературы
1. Sung H., Ferlay J., Siegel R.L., et al. Global Cancer Statistics 2020: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA Cancer J Clin. 2021; 71 (3): 209–49. https://doi.org/10.3322/caac.21660.
2. Каприн А.Д., Старинский В.В., Шахзадова А.О. (ред.) Состояние онкологической помощи населению России в 2021 году. М.: МНИОИ им. П.А. Герцена − филиал ФГБУ «НМИЦ радиологии» Минздрава России; 2022: 239 с.
3. Soerjomataram I., Bray F. Planning for tomorrow: global cancer incidence and the role of prevention 2020–2070. Nat REV Clin Oncol. 2021; 18 (10): 663–72. https://doi.org/10.1038/s41571-021-00514-z.
4. Власина А.Ю., Идрисова Л.Э., Солопова А.Г. и др. Реабилитация онкогинекологических больных после противоопухолевой терапии: пути решения. Акушерство, гинекология и репродукция. 2020; 14 (1): 44–55. https://doi.org/10.17749/2313-7347.2020.14.1.44-55.
5. Кузнецова И.В. (ред.) Адъювантная и альтернативная терапия в акушерстве и гинекологии. М.: ИндексМед Медиа; 2018: 434 с.
6. Contreras N.A., Sabadell J., Verdaguer P., et al. Fertility-sparing approaches in atypical endometrial hyperplasia and endometrial cancer patients: current evidence and future directions. Int J Mol Sci. 2022; 23 (5): 2531. https://doi.org/10.3390/ijms23052531.
7. Кузнецова И.В., Покуль Л.В., Бурчаков Д.И. и др. Терапия и профилактика нарушений здоровья у женщин старше 40 лет. М.: ИндексМед Медиа; 2017: 192 c.
8. Stevenson J.C., Abeyasekera G., Hillyard C.J., et al. Calcitonin and the calcium-regulating hormones in postmenopausal women: effect of oestrogens. Lancet. 1981; 1 (8222): 693–5. https://doi.org/10.1016/s0140-6736(81)91973-5.
9. Доброхотова Ю.Э., Хлынова С.А. Использование лубрикантов при вульвовагинальной атрофии. Русский медицинский журнал. Мать и дитя. 2018; 1 (2): 163–7. https://doi.org/10.32364/2618-84302018-1-2-163-167.
10. Griesser H., Skonietzki S., Fischer T., et al. Low dose estriol pessaries for the treatment of vaginal atrophy: a double-blind placebocontrolled trial investigating the efficacy of pessaries containing 0.2 mg and 0.03 mg estriol. Maturitas. 2012; 71 (4): 360–8. https://doi.org/10.1016/j.maturitas.2011.12.022.
11. Crane T.E., Khulpateea B.R., Alberts D.S., et al. Dietary intake and ovarian cancer risk: a systematic review. Cancer Epidemiol Biomarkers PREV. 2014; 23 (2): 255–73. https://doi.org/10.1158/1055-9965.EPI-130515.
12. Ahmadieh H., Jradi N. Prevalence of menopausal hot flashes in Lebanon: a cross-sectional study. Int J Reprod Biomed. 2021; 19 (9): 789–800. https://doi.org/10.18502/ijrm.v19i9.9711.
13. Kaur H., Merchant M., Haque M.M., Mande S.S. Crosstalk between female gonadal hormones and vaginal microbiota across various phases of women’s gynecological lifecycle. Front Microbiol. 2020; 11: 551. https://doi.org/10.3389/fmicb.2020.00551.
14. Кира Е.Ф. Роль пробиотиков в лечении инфекций влагалища. Российский вестник акушера-гинеколога. 2010; 10 (5): 33–9.
15. Уруймагова А.Т., Прилепская В.Н., Межевитинова Е.А. и др. Бактериальный вагиноз: современные представления о диагностике и лечении. Гинекология. 2021; 23 (4): 286–93. https://doi.org/10.26442/20795696.2021.4.200954.
16. Kushi L.H., Doyle C., McCullough M., et al. American Cancer Society Guidelines on nutrition and physical activity for cancer prevention: reducing the risk of cancer with healthy food choices and physical activity. CA Cancer J Clin. 2012; 62 (1): 30–67. https://doi.org/10.3322/caac.20140.
17. Солопова А.Г., Власина А.Ю., Идрисова Л.Э. и др. Реабилитация онкогинекологических больных: актуальные проблемы и возможные решения. Вестник восстановительной медицины. 2019; 5: 87–96.
18. Солопова А.Г., Идрисова Л.Э., Макацария А.Д. и др. Мультидисциплинарный подход к медицинской реабилитации онкогинекологических больных. Акушерство, гинекология и репродукция. 2017; 11 (4): 57–67. https://doi.org/10.17749/2313-7347.2017.11.4.057-067.
19. Грушина Т.И., Куликов А.Г. Методы физической терапии в реабилитации больных раком молочной железы III клинической группы с постмастэктомическим отеком (часть I). Физиотерапия, бальнеология и реабилитация. 2015; 14 (5): 46–51.
20. Генс Г.П., Сирота Н.А., Олейникова И.Н. Влияние дистресса на качество жизни у больных раком яичников. Злокачественные oпухоли. 2017; 7 (3S1): 166–8.
21. Кузьмина И.В., Раковская Д.Н. Психологическая помощь онкологическим больным на этапах комбинированного лечения. Онкология. Журнал им. П.А. Герцена. 2019; 8 (4): 316–20. https://doi.org/10.17116/onkolog20198041316.
22. Степанова А.М., Мерзлякова А.М., Ткаченко Г.А., Кашия Ш.Р. Физиотерапия, механотерапия и психотерапия в онкологии. Вестник восстановительной медицины. 2016; 5: 42–6.
23. Чевычелова О.Н., Теплоухова Ю.И., Орлова Е.М. Танцевально-двигательная терапия в реабилитации онкологических пациентов. В кн.: Гуляев Г.Ю. (ред.) Научные достижения и открытия 2019: сборник статей X Международного научно-исследовательского конкурса. Пенза: Наука и просвещение; 2019: 216–8.
24. Аржаненкова Л.С., Сычов М.Д. Вопросы трудовой реабилитации в медико-социальной экспертизе онкогинекологических больных. Кубанский научный медицинский вестник. 2007; 1–2: 17–8.
25. Ткаченко Г.А. Арт-терапия в комплексной реабилитации онкологических больных. Физическая и реабилитационная медицина, медицинская реабилитация. 2019; 1 (3): 37–9. https://doi.org/10.36425/2658-6843-2019-3-37-39.
26. Сердюкова Е.Ф. Десенсибилизация и переработка движениями глаз как экспресс-помощь в работе с негативным жизненным опытом. Вестник Костромского государственного университета. Серия: Педагогика. Психология. Cоциокинетика. 2015; 21 (2): 99–101.
27. Chu I.H., Lin Y.J., Wu W.L., et al. Effects of yoga on heart rate variability and mood in women: a randomized controlled trial. J Altern Complement Med. 2015; 21 (12): 789–95. https://doi.org/10.1089/acm.2015.0138.
28. Chu I.H., Wu W.L., Lin I.M., et al. Effects of yoga on heart rate variability and depressive symptoms in women: a randomized controlled trial. J Altern Complement Med. 2017; 23 (4): 310–6. https://doi.org/10.1089/acm.2016.0135.
29. Pauls R.N. Impact of gynecological surgery on female sexual function. Int J Impot Res. 2010; 22 (2): 105–14. https://doi.org/10.1038/ijir.2009.63.
30. Stabile C., Gunn A., Sonoda Y., Carter J. Emotional and sexual concerns in women undergoing pelvic surgery and associated treatment for gynecologic cancer. Transl Androl Urol. 2015; 4 (2): 169–85. https://doi.org/10.3978/j.issn.2223-4683.2015.04.03.
31. Denton A.S., Maher J. Interventions for the physical aspects of sexual dysfunction in women following pelvic radiotherapy. Cochrane Database Syst REV. 2003; 2003 (1): CD003750. https://doi.org/10.1002/14651858.CD003750.
32. Flay L.D., Matthews J.H. The effects of radiotherapy and surgery on the sexual function of women treated for cervical cancer. Int J Radiat Oncol Biol Phys. 1995; 31 (2): 399–404. https://doi.org/10.1016/03603016(94)E0139-B.
33. Reis D., Jones T. Aromatherapy: using essential oils as a supportive therapy. Clin J Oncol Nurs. 2017; 21 (1): 16–9. https://doi.org/10.1188/17.CJON.16-19.
34. Лутошкина М.Г. Физические факторы в комплексном лечении и реабилитации пациентов с хронической венозной недостаточностью. Физиотерапия, бальнеология и реабилитация. 2004; 1: 48–54.
35. Thomaz J.P., Dias T.D.S.M., de Rezende L.F. Effect of taping as treatment to reduce breast cancer lymphedema: literature review. J Vasc Bras. 2018; 17 (2): 136–40. https://doi.org/10.1590/16775449.007217.
36. Потиевская В.И., Шветский Ф.М., Сидоров Д.В. и др. Оценка влияния ксенона на интенсивность послеоперационного болевого синдрома у онкологических пациентов: рандомизированное исследование. Вестник интенсивной терапии им. А.И. Салтанова. 2021; 3: 140–50. https://doi.org/10.21320/1818-474X-2021-3-140-150.
37. Sanders R.D., Ma D., Maze M. Xenon: elemental anaesthesia in clinical practice. Br Med Bull. 2005; 71 (1): 115–35. https://doi.org/10.1093/bmb/ldh034.
38. Кит О.И., Попова Н.Н., Шихлярова А.И. и др. Развитие посткастрационного синдрома и корригирующее действие ксенона в экспоненциальном дозовом режиме у пациенток молодого возраста с онкопатологией репродуктивных органов. Южно-Российский онкологический журнал. 2020; 1 (3): 6–17. https://doi.org/10.37748/2687-0533-2020-1-3-1.
39. Когония Л.М., Новиков Г.А., Орлова Р.В. и др. Практические рекомендации по лечению хронического болевого синдрома у взрослых онкологических больных. Злокачественные oпухоли. 2021; 11 (3s2-2): 167–86. https://doi.org/10.18027/2224-5057-2021-11-3s2-49.
40. Hasan S.S., Vasant D. The emerging new reality of hypnosis teletherapy: a major new mode of delivery of hypnotherapy and clinical hypnosis training. Int J Clin Exp Hypn. 2023; 71 (2): 153–64. https://doi.org/10.1080/00207144.2023.2185527.
41. Hasan S.S., Pearson J.S., Morris J., Whorwell P.J. Skype hypnotherapy for irritable bowel syndrome: effectiveness and comparison with face-to-face treatment. Int J Clin Exp Hypn. 2019; 67 (1): 69–80. https://doi.org/10.1080/00207144.2019.1553766.
42. Котова З.С., Семиглазова Т.Ю., Балдуева И.А. и др. Эфферентная терапия в первой линии лекарственного лечения метастатического колоректального рака. Медицинский cовет. 2018; 10: 172–5. https://doi.org/10.21518/2079-701X-2018-10-172-175.
43. Латипова Д.Х., Проценко С.А., Новик А.В. и др. Место эфферентной терапии в лечении солидных опухолей. Вопросы oнкологии. 2015; 61 (2): 174–9.
44. Gernier F., Ahmed-Lecheheb D., Pautier P., et al. Chronic fatigue, quality of life and long-term side-effects of chemotherapy in patients treated for non-epithelial ovarian cancer: national case-control protocol study of the GINECO-Vivrovaire rare tumors INCa French network for rare malignant ovarian tumors. BMC Cancer. 2021; 21 (1): 1147. https://doi.org/10.1186/s12885-021-08864-8.
45. Deng G. Integrative medicine therapies for pain management in cancer patients. Cancer J. 2019; 25 (5): 343–8. https://doi.org/10.1097/PPO.0000000000000399.
46. Fu T., Guang H.J., Gao X.Z. Percutaneous nerve electrical stimulation for fatigue caused by chemotherapy for cervical cancer. Medicine. 2018; 97 (41): e12020. https://doi.org/10.1097/MD.0000000000012020.
47. Укрепление реабилитации в системах здравоохранения. Всемирная организация здравоохранения. 28 декабря 2022 г. URL: https://apps.who.int/gb/ebwha/pdf_files/EB152/B152_8-ru.pdf (дата обращения 23.06.2023).
48. Самойлова И.Г. Экономическая эффективность реабилитации детей после нейроинфекций. Вятский медицинский вестник. 2019; 1: 64–6.
49. Rehabilitation 2030: a call for action: 6–7 February 2017, Executive Boardroom, WHO Headquarters, Meeting Report. World Health Organization. 2020. URL: https://iris.who.int/handle/10665/339910 (дата обращения 30.09.2023).
50. Солопова А.Е., Чащин А.А., Солопова А.Г., Макацария А.Д. Эпителиальный рак яичников. Клиническая лекция. Акушерство, гинекология и репродукция. 2016; 10 (3): 53–65. https://doi.org/10.17749/2313-7347.2016.10.2.053-065.
51. Walentowicz-Sadlecka M., Grabiec M., Sadlecki P., et al. 25(OH)D3 in patients with ovarian cancer and its correlation with survival. Clin Biochem. 2012; 45 (18): 1568–72. https://doi.org/10.1016/j.clinbiochem.2012.07.110.
52. Seraphin G., Rieger S., Hewison M., et al. The impact of vitamin D on cancer: a mini review. J Steroid Biochem Mol Biol. 2023; 231: 106308. https://doi.org/10.1016/j.jsbmb.2023.106308.
53. Zhang X., Niu W. Meta-analysis of randomized controlled trials on vitamin D supplement and cancer incidence and mortality. Biosci Rep. 2019; 39 (11): BSR20190369. https://doi.org/10.1042/BSR20190369.
54. Южакова Д.В., Ширманова М.В., Сергеева Т.Ф. и др. Иммунотерапия злокачественных новообразований (обзор). Современные технологии в медицине. 2016; 8 (1): 173–82. https://doi.org/10.17691/stm2016.8.1.23.
55. Hoenig H., Nusbaum N., Brummel-Smith K. Geriatric rehabilitation: state of the art. J Am Geriatr Soc. 1997; 45 (11): 1371–81. https://doi.org/10.1111/j.1532-5415.1997.tb02939.x.
56. Солопова А.Г., Табакман Ю.Ю., Идрисова Л.Э., Сдвижков А.М. Реабилитация онкогинекологических больных. Взгляд на проблему. Акушерство, гинекология и репродукция. 2016; 9 (4): 46–54. https://doi.org/10.17749/2070-4968.2015.9.4.046-054.
57. Jacob M.E., Marron M.M., Boudreau R.M., et al. Age, race, and gender factors in incident disability. J Gerontol A Biol Sci Med Sci. 2018; 73 (2): 194–7. https://doi.org/10.1093/gerona/glx194.
58. Основные факторы риска, приводящие к инвалидности в престарелом возрасте, и меры ее профилактики? Всемирная организация здравоохранения. 2003. URL: https://iris.who.int/bitstream/handle/10665/363771/9789289057424-rus.pdf?sequence=1&isAllowed=y (дата обращения 30.09.2023).
59. ICF beginner’s guide: towards a common language for functioning, disability and health. World Health Organization. 2002. URL: https://cdn.who.int/media/docs/default-source/classification/icf/icfbeginnersguide.pdf?sfvrsn=eead63d3_4&download=true (дата обращения 30.09.2023).
60. Chan J.K., Kapp D.S., Shin J.Y., et al. Influence of the gynecologic oncologist on the survival of ovarian cancer patients. Obstet Gynecol. 2007; 109 (6): 1342. https://doi.org/10.1097/01.AOG.0000265207.27755.28.
61. Кулавский В.А., Кулавский Е.В., Зиганшин А.М. Хирургическая менопауза у женщин репродуктивного возраста. Акушерство, гинекология и репродукция. 2017; 10 (4): 105–13. https://doi.org/10.17749/2313-7347.2016.10.4.105-113.
62. Anwar S.L., Adistyawan G., Wulaningsih W., et al. Rehabilitation for cancer survivors: how we can reduce the healthcare service inequality in lowand middle-income countries. Am J Phys Med Rehabil. 2018; 97 (10): 764–71. https://doi.org/10.1097/PHM.0000000000000982.
63. Weare K. Rehabilitation after gynecological cancer treatment. Int J Gynaecol Obstet. 2015; 131 (Suppl. 2): S164–6. https://doi.org/10.1016/j.ijgo.2015.06.015.
64. Falandry C., Fauvet R., Alfonsi P., et al. Combining prehabilitation with enhanced recovery programs in gynecological surgery. J Gynecol Obstet Hum Reprod. 2022; 51 (5): 102376. https://doi.org/10.1016/j.jogoh.2022.102376.
65. Miralpeix E., Mancebo G., Gayete S., et al. Role and impact of multimodal prehabilitation for gynecologic oncology patients in an Enhanced Recovery After Surgery (ERAS) program. Int J Gynecol Cancer. 2019; 29 (8): 1235–43. https://doi.org/10.1136/ijgc-2019-000597.
66. Vonk Noordegraaf A., Anema J.R., van Mechelen W., et al. A personalised eHealth programme reduces the duration until return to work after gynaecological surgery: results of a multicentre randomised trial. BJOG. 2014; 121 (9): 1127–35. https://doi.org/10.1111/1471-0528.12661.
67. Nelson G., Altman A.D., Nick A., et al. Guidelines for postoperative care in gynecologic/oncology surgery: Enhanced Recovery After Surgery (ERAS®) Society recommendations – Part II. Gynecol Oncol. 2016; 140 (2): 323–32. https://doi.org/10.1016/j.ygyno.2015.12.019.
68. Nelson G., Altman A.D., Nick A., et al. Guidelines for preand intraoperative care in gynecologic/oncology surgery: Enhanced Recovery After Surgery (ERAS®) Society recommendations – Part I. Gynecol Oncol. 2016; 140 (2): 313–22. https://doi.org/10.1016/j.ygyno.2015.11.015.
69. Hawkes A.L., Quinn M., Gebski V., et al. Improving treatment for obese women with early stage cancer of the uterus: rationale and design of the levonorgestrel intrauterine device ± metformin ± weight loss in endometrial cancer (feMME) trial. Contemp Clin Trials. 2014; 39 (1): 14–21. https://doi.org/10.1016/j.cct.2014.06.014.
70. Accredited European Training Centres in Gynaecological Oncology. European Society of Gynaecological Oncology. URL: https://esgo.org/esgo-ebcog-accredited-centres/ (дата обращения 11.08.2023).
71. Falcicchio C., Di Lallo D., Fabi A., et al. Use of rehabilitation pathways in women with breast cancer in the first 12 months of the disease: a retrospective study. BMC Cancer. 2021; 21 (1): 311. https://doi.org/10.1186/s12885-021-07927-0.
72. Thorsen L., Gjerset G.M., Loge J.H., et al. Cancer patients’ needs for rehabilitation services. Acta Oncol. 2011; 50 (2): 212–22. https://doi.org/10.3109/0284186X.2010.531050.
73. Butow P.N., Price M.A., Bell M.L., et al. Caring for women with ovarian cancer in the last year of life: a longitudinal study of caregiver quality of life, distress and unmet needs. Gynecol Oncol. 2014; 132 (3): 690–7. https://doi.org/10.1016/j.ygyno.2014.01.002.
74. Seland M., Skrede K., Lindemann K., et al. Distress, problems and unmet rehabilitation needs after treatment for gynecological cancer. Acta Obstet Gynecol Scand. 2022; 101 (3): 313–22. https://doi.org/10.1111/aogs.14310.
75. Holm L.V., Hansen D.G., Kragstrup J., et al. Influence of comorbidity on cancer patients’ rehabilitation needs, participation in rehabilitation activities and unmet needs: a population-based cohort study. Support Care Cancer. 2014; 22 (8): 2095–105. https://doi.org/10.1007/s00520-014-2188-1.
Об авторе
А. Г. АлександровРоссия
Александров Андрей Георгиевич - к.б.н. Scopus Author ID: 57211350219.
Ул. Садовая-Триумфальная, д. 4/10, Москва 127006; ул. Быкова, д. 84Б, Ленинградская обл., Всеволожский р-н, Колтушское с/п, с. Павлово 188680
Рецензия
Для цитирования:
Александров А.Г. Организация реабилитации при злокачественных новообразованиях репродуктивной системы. Реабилитология. 2024;2(2):247-263. https://doi.org/10.17749/2949-5873/rehabil.2024.22
For citation:
Aleksandrov A.G. Organization of rehabilitation for reproductive system malignant neoplasms. Journal of Medical Rehabilitation. 2024;2(2):247-263. (In Russ.) https://doi.org/10.17749/2949-5873/rehabil.2024.22






