Перейти к:
Оценка эффективности и безопасности ритмической периферической магнитной стимуляции у пациентов с пояснично-крестцовой радикулопатией в раннем реабилитационном периоде после микродискэктомии
https://doi.org/10.17749/2949-5873/rehabil.2024.23
Аннотация
Актуальность. Значительный объем хирургической активности для лечения дискогенной радикулопатии на поясничном уровне повышает актуальность совершенствования комплексных послеоперационных реабилитационных программ, включающих инновационные физиотерапевтические методики. Один из современных и безопасных методов
физиотерапевтической реабилитации – ритмическая периферическая магнитная стимуляция (рПМС).
Цель: оценить эффективность реабилитационного лечения с включением курса рПМС у пациентов с пояснично-крестцовой радикулопатией (ПКР) в раннем реабилитационном периоде после микродискэктомии.
Материал и методы. В проспективном рандомизированном сравнительном исследовании принял участие 71 пациент с ПКР после микродискэктомии. На 7-й день после операции больные были рандомизированы на две группы. В 1-й группе (n=35) пациенты получали курс рПМС в дополнение к традиционной реабилитационной терапии, во 2-й группе (n=36) – только традиционную терапию. Оценку болевого синдрома проводили по визуально-аналоговой шкале, тревожности – по опроснику Спилбергера–Ханина, качества жизни – по опроснику EuroQol-5D.
Результаты. На 21-й день реабилитационного лечения зарегистрировано статистически значимое (p=0,036) различие между результатами в 1-й и 2-й группах по интенсивности боли в нижней конечности. На 21-й день выявлено статисти-
чески значимое различие (р=0,042) между группами по частоте распределения тяжести личностной тревожности. В 1-й группе было достигнуто статистически значимое различие частот распределения уровня самообслуживания на 21-й день курса терапии в сравнении с данными на 7-й день (p<0,05).
Заключение. Полученные клинические эффекты в отношении регресса болевого синдрома, улучшения чувствительности и психологического состояния пациентов были более значительными в группе, которая получала курс рПМС. Результаты нашей работы показывают, что включение рПМС в реабилитационное послеоперационное лечение может стать полезным инструментом для улучшения восстановления больных.
Ключевые слова
Для цитирования:
Блохина В.Н. Оценка эффективности и безопасности ритмической периферической магнитной стимуляции у пациентов с пояснично-крестцовой радикулопатией в раннем реабилитационном периоде после микродискэктомии. Реабилитология. 2024;2(3):277–285. https://doi.org/10.17749/2949-5873/rehabil.2024.23
For citation:
Blokhina V.N. Efficacy and safety of repetitive peripheral magnetic stimulation in patients with lumbosacral radiculopathy during early postoperative rehabilitation period following microdiscectomy. Journal of Medical Rehabilitation. 2024;2(3):277–285. (In Russ.) https://doi.org/10.17749/2949-5873/rehabil.2024.23
ВВЕДЕНИЕ / INTRODUCTION
Пояснично-крестцовая радикулопатия (ПКР) представляет собой повреждение поясничных или первого крестцового спинномозговых корешков, обусловленное патологией межпозвонкового диска [1][2]. ПКР характеризуется выраженным и продолжительным болевым синдромом, чувствительными нарушениями в соответствующих дерматомах и/или слабостью в соответствующих миотомах (индикаторных мышцах), снижением коленного или ахиллова рефлексов.
Важно отметить, что болевой синдром при радикулопатии отличается высокой интенсивностью и может приобретать хронический характер, что затрудняет процесс выздоровления и ухудшает качество жизни (КЖ) пациентов [3][4].
В настоящее время есть свидетельства, что при неэффективном консервативном лечении дискогенной ПКР в течение 6–8 нед рекомендовано хирургическое вмешательство [5][6]. На сегодняшний день микродискэктомия является общепризнанным и наиболее распространенным методом оперативного лечения дискогенной ПКР [7][8]. Однако после микрохирургических операций по поводу радикулопатии сохраняется риск развития повторной грыжи межпозвонкового диска, возобновления болевого синдрома, более медленного восстановления пациентов [9][10]. Следует учитывать эти данные для формирования программ реабилитации больных после микрохирургических вмешательств.
Инновационные методы физиотерапевтического лечения могут быть рассмотрены в качестве дополнительного инструмента реабилитационной программы. Одним из таких методов является ритмическая периферическая магнитная стимуляция (рПМС). Многолетний опыт использования рПМС продемонстрировал ее безопасность для пациентов. Это имеет особое значение для больных с радикулопатией вследствие того, что длительные курсы лекарственной терапии при данном заболевании повышают риск развития побочных эффектов [11].
При рПМС используется импульсное магнитное поле, воздействие которого осуществляется на проводящие структуры периферической нервной системы (ПНС) [12][13]. Спинномозговые нервы и внутримышечные аксоны – элементы ПНС, возбуждение которых происходит в ответ на магнитную стимуляцию [14][15].
Применение рПМС безболезненно. Это объясняется тем, что болевые рецепторы кожи стимулируются минимально, но магнитный импульс проникает на необходимую глубину для активации нервных структур [16]. Такие характеристики, как мощность стимулятора, форма, размер индуктора, определяют возможность глубины воздействия магнитного импульса [17].
За более чем 20-летнюю историю изучения рПМС клиническая эффективность метода была продемонстрирована в ряде исследований. Следует отметить, что снижение уровня боли при применении данной методики наблюдалось у пациентов с миофасциальным болевым синдромом [18], при терапии острой люмбалгии [19], у больных с хроническим болевым синдромом в спине [12][20][21], нейропатической болью [22], синдромом оперированного позвоночника [23]. Улучшение тазовых функций было зарегистрировано у пациентов с нейрогенными расстройствами мочеиспускания в раннем реабилитационном периоде после операции [24]. Положительный клинический эффект в виде уменьшения интенсивности болевого синдрома и улучшения функционального статуса больных отмечен в лечении пациентов с поясничной радикулопатией [25]. Следует подчеркнуть, что больные хорошо переносят процедуру рПМС, без ощущения дискомфорта или болезненности [26].
Цель – оценить эффективность реабилитационного лечения с включением курса рПМС у пациентов с ПКР в раннем реабилитационном периоде после микродискэктомии.
МАТЕРИАЛ И МЕТОДЫ / MATERIAL AND METHODS
На базе ФГБУ «Национальный медико-хирургический центр им. Н.И. Пирогова» Минздрава России в 2014–2017 гг. проведено проспективное рандомизированное сравнительное исследование с участием 71 пациента с ПКР, которым было выполнено микрохирургическое вмешательство.
Критерии включения и исключения / Inclusion and exclusion criteria
При формировании когорты пациентов использовали следующие критерии включения:
– возраст 18 лет и старше;
– клинически подтвержденный диагноз радикулопатии на поясничном уровне (повреждение корешков L5, S1) с наличием соответствующих изменений по данным нейровизуализации (грыжи межпозвонковых дисков на уровнях L4–L5, L5–S1);
– проведенное оперативное лечение (микродискэктомия);
– наблюдение в течение 3 нед (ранний реабилитационный период).
Критерии исключения:
– беременность;
– намагничивающиеся металлические предметы в теле пациента, наличие которых служит противопоказанием для проведения магнитной стимуляции;
– наличие имплантированного устройства для управления физиологическими функциями (кардиостимулятор, нейростимулятор).
Участники исследования / Study participants
В исследовании принял участие 71 пациент с ПКР – 44 (61,9%) мужчины и 27 (38,1%) женщин. Средний возраст больных составил 46,8±10,5 года, средняя продолжительность заболевания – 6,3±4,1 года, средняя продолжительность обострения радикулопатии – 2,8±0,9 мес. Важно отметить, что 83% пациентов были молодого и среднего возраста – от 20 до 59 лет.
На 7-й день после микродискэктомии пациенты были рандомизированы методом случайного распределения на две группы. В 1-ю группу вошли 35 больных, реабилитационное лечение которых включало традиционную терапию и курс рПМС, 2-ю группу составили 36 участников, которые получали традиционное лечение без курса рПМС. Пациенты обеих групп были однородны по показателям: пол, возраст, длительность заболевания, клинические и психологические характеристики. Достоверных межгрупповых различий выявлено не было (р>0,05).
Методы обследования / Examination methods
Первичное обследование пациентов осуществляли на 7-й день, повторное – на 21-й день после операции.
Клинико-неврологическое обследование включало применение визуально-аналоговой шкалы (ВАШ) для объективизации болевых ощущений, шкалы тревожности Спилбергера–Ханина, опросника EuroQol-5D для оценки КЖ больных. Специальный опросник по безопасности использования магнитной стимуляции заполняли все пациенты, которые получали курс рПМС [26].
Нейровизуализацию (магнитно-резонансную томографию) выполняли всем больным для верификации дископатии.
У пациентов с двигательными нарушениями проводили комплексное нейрофизиологическое обследование для изучения функционального состояния нервно-мышечной системы.
Методы терапии / Therapy methods
Традиционная терапия
Для традиционной терапии применяли лекарственные средства (нестероидные противовоспалительные препараты, миорелаксанты центрального действия, препараты противосудорожного действия), лечебную физкультуру, процедуры физиотерапии (низкоинтенсивное лазерное излучение, фонофорез с гидрокортизоном, массаж).
Магнитная стимуляция
Применяли магнитный стимулятор «Нейрософт» (ООО «Нейрософт», Россия) с исходной мощностью 2,0 Тл и кольцевым индуктором диаметром 125 мм. Стимулятор был соединен с электромиографом, с помощью которого записывали результаты вызванного моторного ответа (ВМО) с тестовых мышц. Направление электрического тока в индукторе было краниальным [17].
Интенсивность магнитного стимула определяли в зависимости от индивидуального порога ВМО, который является показателем стимуляции спинномозговых корешков при рПМС [27]. Для регистрации индивидуального порога ВМО для каждого пациента фиксировали минимальную интенсивность магнитного импульса, определяемую в процентах (более чем в 50% повторных стимулов при рПМС был определен ВМО с мышцы-мишени амплитудой более 50 мкВ). Тестовые мышцы для регистрации порога ВМО: короткий разгибатель пальцев стопы у пациентов с радикулопатией L5 и мышца, отводящая большой палец стопы, у больных с радикулопатией S1 [17].
Во время выполнения процедуры пациенты комфортно располагались на кушетке в положении лежа на животе. В случаях клинических проявлений радикулопатии в виде болевого синдрома и чувствительных расстройств мы применяли первый протокол магнитной стимуляции. Центр индуктора находился на расстоянии 3–4 см от остистых отростков позвонков L3–L4 в сторону поврежденного корешка (при радикулопатии L5), при повреждении корешка S1 центр койла помещали на расстояние 3–4 см от основания крестца [17]. Схема расположения индуктора при радикулопатии L5 представлена на рисунке 1. Параметр «интенсивность» магнитного стимула подбирали для каждого участника после регистрации порога ВМО. Средний порог ВМО соответствовал 32,8±3,7% от исходной мощности стимулятора. Интенсивность была выше порога ВМО на 10–15%, для регистрации предельного уровня данного параметра ориентировались на восприятие пациентом процедуры стимуляции. Использовали низкочастотную стимуляцию с частотой 1 Гц. Другие параметры стимуляции: в трейне 100 стимулов, пауза в течение 5 с, 1500 импульсов в одной сессии (процедуре), продолжительность сессии 25 мин, всего проводили 10 сессий для каждого пациента.
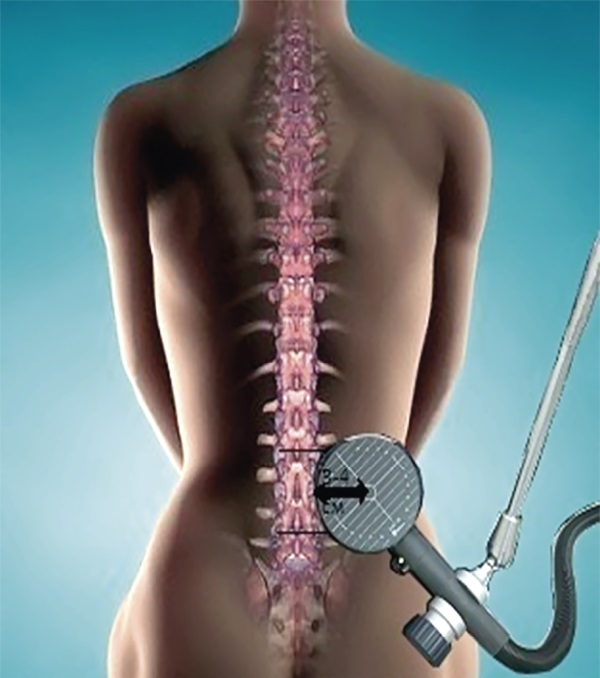
Рисунок 1. Схема расположения индуктора при радикулопатии L5
Figure 1. Arrangement of the inductor in L5 radiculopathy
Больным, у которых была диагностирована мышечная слабость при тыльном сгибании стопы (радикулопатия L5), подошвенном сгибании стопы и пальцев (радикулоптия S1), проводили первый и второй варианты протокола магнитной стимуляции. Параметры второго протокола: частота 1 Гц, общее количество импульсов в одной сессии 1200, продолжительность процедуры 20 мин. Индуктор помещали на заднюю область коленного сустава, для определения необходимой интенсивности магнитного импульса оценивали ощущения пациента. Процент интенсивности магнитного стимула подбирали таким образом, чтобы вызвать движения в стопе в виде сгибания-разгибания. Количество процедур при проведении второго протокола составляло 10 для каждого больного.
Статистический анализ / Statistical analysis
Статистический анализ результатов исследования осуществляли с помощью пакета программы SPSS Statistics 21 (IBM, США). Количественные данные приведены в виде средних значений и стандартных отклонений, для категориальных показателей рассчитаны абсолютные и относительные (%) частоты встречаемости. Межгрупповые различия оценивали с помощью теста Манна–Уитни, для связанных выборок использовали критерий Уилкоксона. Взаимосвязь категориальных данных для межгрупповых и связанных выборок определяли с помощью критерия χ² Пирсона и точного критерия Фишера в случае малых (<5) значений ожидаемых частот. Различия на уровне значимости p<0,05 определяли как статистически достоверные.
РЕЗУЛЬТАТЫ / RESULTS
Первичное обследование / Primary examination
Болевой синдром
Все участники исследования испытывали болевые ощущения на 7-й день после оперативного вмешательства. Оценка боли в нижней части спины по ВАШ в 1-й группе составила 3,2±1,1 балла, во 2-й – 3,02±1,2 балла. Болевой синдром в нижней конечности у пациентов 1-й группы оценен в 2,2±1,0 балла, 2-й группы – в 2,2±1,0 балла (табл. 1).
Таблица 1. Динамика уровня болевого синдрома в группах исследования (оценка по визуально-аналоговой шкале), баллы
Table 1. Dynamics of pain intensity in the study groups (visual analog scale), score
Локализация боли / Localization of pain | 1-я группа / Group 1 (n=35) | 2-я группа / Group 2 (n=36) | ||
7-й день / Day 7 | 21-й день / Day 21 | 7-й день / Day 7 | 21-й день / Day 21 | |
Боль в спине / Back pain | 3,2±1,1 | 1,8±0,6* | 3,02±1,2 | 1,8±0,7* |
Боль в нижней конечности / Lower limb pain | 2,2±1,05 | 1,2±0,4** | 2,05±0,8 | 1,5±0,5* |
Примечание. * Статистически значимые различия между 7-м и 21-м днями (р<0,05 по критерию Уилкоксона). ** Статистически значимые различия между группами (р=0,036 по критерию Манна–Уитни).
Note. * Statistically significant differences between Days 7 and 21 (p<0.05, Wilcoxon test). ** Statistically significant differences between groups (p=0.036, Mann–Whitney test).
Гипестезию болевой чувствительности в дерматоме поврежденного корешка в 1-й группе испытывали 28 (80%) пациентов, во 2-й группе – 27 (75%). Гиперестезия в соответствующих дерматомах была отмечена у 2 (5,7%) и 2 (5,6%) больных в 1-й и 2-й группах соответственно. Выпадение ахиллова рефлекса зафиксировано у пациентов с повреждением корешка S1: у 10 (28,5%) участников 1-й группы и у 11 (30,5%) больных 2-й группы. Мышечная слабость при тыльном сгибании стопы и подошвенном сгибании стопы и пальцев обнаружена у 15 (42,8%) и 17 (47,2%) пациентов в 1-й и 2-й группах соответственно. При проведении комплексного электромиографического обследования у больных с мышечной слабостью были выявлены признаки радикулярного повреждения мышц аксонального характера (зона иннервации L5–S1) в стадии хронического процесса.
Уровень тревожности
При исследовании степени тревожности по шкале Спилбергера–Ханина на 7-й день после оперативного вмешательства было зарегистрировано наличие ситуационной тревожности (СТ) у 100% участников, причем 8 (11,2%) пациентов имели высокий уровень СТ. Следует отметить, что высокая личностная тревожность (ЛТ) выявлена у 9 (25,72%) больных в 1-й группе и у 9 (25%) пациентов во 2-й группе. Умеренная ЛТ определена у 24 (68,57%) и 25 (69,44%) участников в 1-й и 2-й группах соответственно (табл. 2).
Таблица 2. Динамика уровня личностной тревожности (ЛТ) в группах исследования (оценка по шкале Спилбергера–Ханина), n (%)
Table 2. Dynamics of trait anxiety (TA) level in the study groups (state-trait anxiety inventory), n (%)
Уровень ЛТ / TA level | 1-я группа / Group 1 (n=35) | 2-я группа / Group 2 (n=36) | ||
7-й день / Day 7 | 21-й день / Day 21 | 7-й день / Day 7 | 21-й день / Day 21 | |
Низкий / Low | 2 (5,71) | 20 (57,14)* | 2 (5,56) | 12 (33,33) |
Умеренный / Moderate | 24 (68,57) | 14 (40,00)* | 25 (69,44) | 24 (66,67) |
Высокий / High | 9 (25,71) | 1 (2,86)* | 9 (25,00) | 0 (0,00) |
Примечание. * Статистически значимое различие частот распределения уровня ЛТ в 1-й группе в сравнении с данными во 2-й группе на 21-й день (p=0,042 по точному критерию Фишера).
Note. * Statistically significant difference in the frequency distribution of TA levels between Groups 1 and 2 on Day 21 (p=0.042, Fisher exact p value).
Качество жизни
Данные оценки показателей КЖ больных на 7-й день после операции по опроснику EuroQol-5D продемонстрировали наличие изменений по всем параметрам, включая «боль» и «самообслуживание». Большинство пациентов определили свои нарушения как умеренные. По показателю «самообслуживание» (возможность ухода за собой) 33 (94,3%) участника в 1-й группе и 34 (94,4%) во 2-й группе оценили нарушения как умеренные, 2 (5,7%) пациента в 1-й группе и 2 (5,6%) во 2-й группе отметили выраженную степень нарушений. По показателю «боль» 30 (85,7%) больных в 1-й группе и 30 (83,3%) во 2-й группе определили умеренный характер нарушений, 3 (8,6%) пациента в 1-й группе и 4 (11,1%) во 2-й группе охарактеризовали ощущения боли как выраженные. При этом 2 (5,7%) участника в 1-й группе и 2 (5,6%) во 2-й группе в разделе «боль» выбрали ответ «нет нарушений» (табл. 3).
Таблица 3. Динамика показателей качества жизни по опроснику EuroQol-5D (разделы «самообслуживание», «боль/дискомфорт») в группах исследования, n (%)
Table 3. Dynamics of health-related quality of life (EuroQol-5D questionnaire, Self-care and Pain/Discomfort sections) in the study groups, n (%)
Нарушения / Disability | 1-я группа / Group 1 (n=35) | 2-я группа / Group 2 (n=36) | ||
7-й день / Day 7 | 21-й день / Day 21 | 7-й день / Day 7 | 21-й день / Day 21 | |
Самообслуживание / Self-care | ||||
нет / no | 0 (0,0) | 14 (40,0)* | 0 (0,0) | 9 (25,0) |
умеренные / moderate | 33 (94,3) | 19 (54,3)* | 34 (94,4) | 25 (69,4) |
выраженные / severe | 2 (5,7) | 2 (5,7)* | 2 (5,6) | 2 (5,6) |
Боль/дискомфорт // Pain/Discomfort | ||||
нет / no | 2 (5,7) | 19 (54,3)** | 2 (5,6) | 14(38,9)** |
умеренные / moderate | 30 (85,7) | 16 (45,7)** | 30 (83,3) | 22 (61,1)** |
выраженные / severe | 3 (8,6) | 0 (0,0)** | 4 (11,1) | 0 (0,0)** |
Примечание. * Статистически значимые различия частот распределения уровня самообслуживания в 1-й группе на 21-й день в сравнении с данными на 7-й день (р<0,05 по критерию χ² Пирсона). ** Статистически значимые различия частот распределения уровня боли на 21-й день в сравнении с данными на 7-й день (р<0,05 по критерию χ² Пирсона).
Note. * Statistically significant differences in the frequency distribution of self-care level in Groups 1 and 2 between Days 7 and 21 (p<0.05, Pearson's χ² test). ** Statistically significant differences in the frequency distribution of pain intensity between Days 7 and 21 (p<0.05, Pearson's χ² test).
Повторное обследование / Repeated examination
Болевой синдром, чувствительные и двигательные нарушения
На 21-й день курса реабилитационного лечения у всех участников исследования в обеих группах было отмечено снижение уровня болевого синдрома в нижней части спины и конечностях. У 100% пациентов расширился объем движений, увеличилась длительность безболевой ходьбы, повысились возможности ухода за собой в сравнении с тестированием на 7-й день. В 1-й группе зарегистрировано статистически значимое различие результатов интенсивности боли в нижней конечности в сравнении с данными, полученными при обследовании больных во 2-й группе (p=0,036 по критерию Манна–Уитни) (см. табл. 1).
Полное восстановление болевой чувствительности в соответствующих дерматомах зафиксировано у 3 (8,5%) больных в 1-й группе и у 1 (2,7%) пациента во 2-й группе. У 6 (17,1%) и 3 (8,3%) участников 1-й и 2-й групп соответственно отмечено появление гиперестезии (при первом тестировании у них была выявлена гипестезия в зоне иннервации поврежденных корешков). При статистической обработке результатов восстановления чувствительных нарушений получено достоверное различие (p=0,012 по критерию χ²) у больных в 1-й группе на 21-й день в сравнении с тестированием на 7-й день.
Следует отметить, что у пациентов с наличием мышечной слабости в стопе не было отмечено достоверного улучшения на 21-й день после оперативного вмешательства, что свидетельствует о хроническом генезе радикулярного поражения.
Уровень тревожности
Уменьшение результатов по параметрам СТ и ЛТ зарегистрировано у пациентов в обеих группах в сравнении с тестированием на 7-й день лечения (р<0,05 по критерию Уилкоксона). Только 1 (2,8%) больной в 1-й группе имел высокую степень ЛТ. При анализе показателей ЛТ у участников обеих групп зафиксировано значимое различие в оценке показателей тяжести тревожности в пользу 1-й группы на 21-й день реабилитационного лечения в сравнении с данными во 2-й группе (р=0,042, точный критерий Фишера) (см. табл. 2).
Число пациентов с СТ высокой и умеренной степеней снизилось на 21-й день после микродискэктомии. Следует отметить, что достоверного различия между показателями распределения тяжести СТ в 1-й и 2-й группах на 21-й день тестирования не зарегистрировано (р=0,872 по критерию χ²).
Качество жизни
Оценка КЖ больных продемонстрировала, что были достигнуты статистически значимые результаты в разделах «самообслуживание», «боль/дискомфорт».
Значительно уменьшилось количество пациентов с умеренными нарушениями самообслуживания, 14 (40%) участников в 1-й группе и 9 (25%) во 2-й группе отрицали наличие проблем с самообслуживанием на 21-й день терапии. В 1-й группе получено статистически значимое различие частот распределения уровня самообслуживания на 21-й день курса реабилитационного лечения в сравнении с данными на 7-й день (p<0,05 по критерию χ²). Достоверные изменения при изучении раздела «боль/дискомфорт» опросника КЖ были зафиксированы у больных в обеих группах на 21-й день после оперативного вмешательства по сравнению с данными на 7-й день (р<0,05 по критерию χ²) (см. табл. 3).
Улучшение по данным разделов «повседневная активность», «мобильность», «беспокойство/депрессия» опросника EuroQol-5D было получено у больных в обеих группах при проведении второго тестирования, при этом изменения не были статистически значимыми.
ОБСУЖДЕНИЕ / DISCUSSION
В нашем исследовании изучалась возможность улучшения эффективности реабилитационного лечения больных с радикулопатией после оперативного вмешательства с помощью дополнительного курса физиотерапевтической методики рПМС. Пациенты обеих групп отметили хорошую переносимость реабилитационного лечения в течение периода наблюдения. Больные, получавшие рПМС, сообщили об отсутствии болезненности во время проведения процедур.
Зарегистрированное достоверное уменьшение интенсивности болевого синдрома у пациентов в 1-й группе на 21-й день лечения следует оценивать как небольшое, но существенное клиническое улучшение при дополнительном применении рПМС. Статистически значимое восстановление чувствительности, достигнутое в 1-й группе, также свидетельствует о преимуществе использования изучаемой методики. Влияние рПМС на болевой синдром у пациентов с острой и хронической болью в спине может быть обусловлено эффектом магнитной стимуляции на периферическом уровне. Данный эффект развивается за счет ингибирования деполяризации тонких С-волокон, которые являются проводниками болевой чувствительности, и активации деполяризации толстых миелиновых волокон. Воздействие магнитной стимуляции на триггерные точки также имеет значение [16, 18]. В исследованиях, в которых показана способность рПМС оказывать влияние на возбудимость сенсомоторной коры у пациентов с болевым синдромом в спине, была использована магнитная стимуляция с частотой 20 Гц, общее число импульсов при проведении одной процедуры рПМС составило 15 тыс. [28]. Результаты, полученные в нашей работе, согласуются с данными других исследователей, которые применяли импульсную магнитную стимуляцию при хронической боли в спине [12][13].
При оценке улучшения психологического состояния пациентов на 21-й день в 1-й группе только у 1 (2,8%) больного зафиксирован высокий уровень ЛТ, у 17 (23,9%) пациентов уровень ЛТ понизился до умеренного и низкого. Уменьшение ЛТ следует расценивать как важное достижение, поскольку, согласно результатам C. D’Angelo et al. (2010 г.) [29], высокая степень ЛТ увеличивает риск хронизации боли после хирургического лечения радикулопатии на поясничном уровне.
Анализ влияния рПМС на КЖ пациентов в период послеоперационного лечения после микрохирургического вмешательства с применением опросника EuroQol-5D ранее не проводился. Данный опросник является надежным и сопоставимым в сравнительных исследованиях для изучения КЖ у больных после спинальной хирургии [30]. Полученные результаты продемонстрировали достоверное улучшение возможности ухода за собой в группе больных, которые получали рПМС. Следует отметить, что для оценки других параметров КЖ, в особенности «тревога/депрессия», требуется более длительное наблюдение. В работе D. Lubelski et al. (2015 г.) КЖ пациентов изучали через 1 год после дискэктомии на поясничном уровне [31].
Принимая во внимание полученные клинические эффекты в отношении регресса болевого синдрома, улучшения чувствительности и психологического состояния пациентов, которые дополнительно получали курс рПМС в рамках реабилитационной программы после микродискэктомии, можно сделать вывод о скромном, но статистически значимом преимуществе применения данной методики. Хорошая переносимость, отсутствие болезненности при проведении процедуры является ценным качеством рПМС.
Ограничения исследования / Limitations of the study
В исследование не была включена контрольная группа, что является ограничительным фактором проведенного эксперимента. Учитывая это ограничение, полученные результаты следует рассматривать как предварительные, требуется проведение контролируемых исследований для дальнейшего изучения эффективности рПМС.
ЗАКЛЮЧЕНИЕ / CONCLUSION
Более чем 20-летняя история применения рПМС и достигнутые успехи в терапии пациентов с болью в спине, ПКР при осуществлении реабилитационных программ после оперативных вмешательств позволяют рассматривать этот метод как ценный терапевтический инструмент. Безопасность проведения рПМС доказана многолетним стажем ее использования и подчеркивает перспективность и необходимость дальнейшего изучения для повышения результативности реабилитации.
Список литературы
1. Ropper A.H., Zafonte R.D. Sciatica. N Engl J Med. 2015; 372 (13): 1240–8. https://doi.org/10.1056/nejmra1410151.
2. Dydyk A.M., Khan M.Z., Singh P. Radicular back pain. StatPearls. Treasure Island (FL): StatPearls Publishing; 2019: 2022 Oct 24.
3. Konstantinou K., Hider S.L., Jordan J.L., et al. The impact of low backrelated leg pain on outcomes as compared with low back pain alone: a systematic review of the literature. Clin J Pain. 2013; 29 (7): 644–54. https://doi.org/10.1097/AJP.0b013e31826f9a52.
4. Benditz A., Madl M., Loher M., et al. Prospective medium-term results of multimodal pain management in patients with lumbar radiculopathy. Sci Rep. 2016; 6: 28187. https://doi.org/10.1038/srep28187.
5. Alentado V.J., Lubelski D., Steinmetz M.P., et al. Optimal duration of conservative management prior to surgery for cervical and lumbar radiculopathy: a literature review. Spine. 2014; 4 (4): 279–86. https://doi.org/10.1055/s-0034-1387807.
6. Gadjradj P.S., Arts M.P., van Tulder M.W., et al. Management of symptomatic lumbar disk herniation: an international perspective. Spine. 2017; 42 (23): 1826–34. https://doi.org/10.1097/ BRS.0000000000002294.
7. Seiger A., Gadjradj P.S., Harhangi B.S., et al. PTED study: design of a non-inferiority, randomised controlled trial to compare the effectiveness and cost-effectiveness of percutaneous transforaminal endoscopic discectomy (PTED) versus open microdiscectomy for patients with a symptomatic lumbar disc herniation. BMJ Open. 2017; 7 (12): e018230. https://doi.org/10.1136/bmjopen-2017-018230.
8. Kim S.K., Kang S.S., Hong Y.H., et al. Clinical comparison of unilateral biportal endoscopic technique versus open microdiscectomyfor single-level lumbar discectomy: a multicenter, retrospective analysis. J Orthop Surg Res. 2018; 13 (1): 22. https://doi.org/10.1186/s13018018-0725-1.
9. Heindel P., Tuchman A., Hsieh P., et al. Reoperation rates following single-level lumbar discectomy. Spine. 2017; 42 (8): E496–501. https://doi.org/10.1097/BRS.0000000000001855.
10. Amirdelfan K., Webster L., Poree L., et al. Treatment options for failed back surgery syndrome (FBSS) patients with refractory chronic pain: an evidence-based approach. Spine. 2017; 42 (Suppl. 14): S41–52. https://doi.org/10.1097/BRS.0000000000002217.
11. Журавлева М.В., Кукес В.Г., Прокофьев А.Б. и др. Рациональное применение НПВП – баланс эффективности и безопасности (обзор литературы). Международный журнал прикладных и фундаментальных исследований. 2016; 6-4: 687–96.
12. Massé-Alarie H., Flamand V., Moffet H., Schneider C. Peripheral neurostimulation and specific motor training of deep abdominal muscles improve posturomotor control in chronic low back pain. Clin J Pain. 2013; 29 (9): 814–23. https://doi.org/10.1097/AJP.0b013e318276a058.
13. Beaulieu L., Schneider C. Repetitive peripheral magnetic stimulation to reduce pain or improve sensorimotor impairments: a literature review on parameters of application and afferents recruitment. Neurophysiol Clin. 2015; 45 (3): 223–37. https://doi.org/10.1016/j.neucli.2015.08.002.
14. Никитин С.С., Куренков А.Л. Методические основы транскраниальной магнитной стимуляции в неврологии и психиатрии. М.: ИПЦ Маска; 2006: 167 с. Nikitin S.S., Kurenkov A.L. Methodological foundations of transcranial magnetic stimulation in neurology and psychiatry. Moscow: IPTs Maska; 2006: 167 pp. (in Russ.).
15. Babbs C.F. A compact theory of magnetic nerve stimulation: predicting how to aim. Biomed Eng Online. 2014; 13: 53. https://doi.org/10.1186/1475-925X-13-53.
16. Struppler A., Angerer B., Gündisch C., Havel P. Modulatory effect of repetitive peripheral magnetic stimulation on skeletal muscle tone in healthy subjects: stabilization of the elbow joint. Exp Brain Res. 2004; 157 (1): 59–66. https://doi.org/10.1007/s00221-003-1817-6.
17. Николаев С.Г. Электромиография: клинический практикум. Иваново: ПресСто; 2013: 394 с.
18. Smania N., Corato E., Fiaschi A., et al. Repetitive magnetic stimulation: a novel therapeutic approach for myofascial pain syndrome. J Neurol. 2005; 252 (3): 307–14. https://doi.org/10.1007/s00415-005-0642-1.
19. Lim Y.H., Song J.M., Choi E.H., Lee J.W. Effects of repetitive peripheral magnetic stimulation on patients with acute low back pain: a pilot study. Ann Rehabil Med. 2018; 42 (2): 229–38. https://doi.org/10.5535/arm.2018.42.2.229.
20. Massé-Alarie H., Beaulieu L.D., Preuss R., Schneider C. Repetitive peripheral magnetic neurostimulation of multifidus muscles combined with motor training influences spine motor control and chronic low back pain. Clin Neurophysiol. 2017; 128 (3): 442–53. https://doi.org/10.1016/j.clinph.2016.12.020.
21. Yan T., Liang M., Peng J., et al. Cortical mechanisms underlying effects of repetitive peripheral magnetic stimulation on dynamic and static postural control in patients with chronic non-specific low back pain: a double-blind randomized clinical trial. Pain Ther. 2024; 13 (4): 953–70. https://doi.org/10.1007/s40122-024-00613-6.
22. Kumru H., Albu S., Vidal J., Tormos J.M. Effectiveness of repetitive trancranial or peripheral magnetic stimulation in neuropathic pain. Disabil Rehabil. 2017; 39 (9): 856–66. https://doi.org/10.3109/09638288.2016.1170213.
23. Гореликов А.Е., Мельникова Е.А., Разумов А.Н. и др. Реабилитация больных с синдромом оперированного позвоночника с осложненным течением послеоперационного периода после дискэктомии. Вопросы курортологии, физиотерапии и лечебной физической культуры. 2017; 94 (5): 40–7. https://doi.org/10.17116/kurort201794540-47.
24. Бородулина И.В., Рачин А.П., Бадалов Н.Г., Гуща А.О. Периферическая ритмическая магнитная стимуляция при нейрогенных расстройствах мочеиспускания: обзор литературы и результаты клинического исследования. Нервно-мышечные болезни. 2017; 7 (2): 54–66. https://doi.org/10.17650/2222-87212017-7-2-54-66.
25. Savulescu S.E., Berteanu M., Filipescu I., et al. Repetitive peripheral magnetic stimulation (rPMS) in subjects with lumbar radiculopathy: an electromyography-guided prospective, randomized study. In Vivo. 2021; 35 (1): 623–7. https://doi.org/10.21873/invivo.12300.
26. Rossi S., Hallett M., Rossini P.M., Pascual-Leone A. Safety, ethical considerations, and application guidelines for the use of transcranial magnetic stimulation in clinical practice and research. Clin Neurophysiol. 2009; 120 (12): 2008–39. https://doi.org/10.1016/j.clinph.2009.08.016.
27. Блохина В.Н., Кузнецов А.Н., Виноградов О.И. и др. Сравнительный анализ возбудимости корешковой внутримышечной аксональной систем у здоровых добровольцев при периферической магнитной стимуляции. Нервно-мышечные болезни. 2017; 7 (2): 48–53. https://doi.org/10.17650/2222-8721-2017-7-2-48-53.
28. Massé-Alarie H., Schneider C. Revisiting the corticomotor plasticity in low back pain: challenges and perspectives. Healthcare. 2016; 4 (3):67. https://doi.org/10.3390/healthcare4030067.
29. D'Angelo C., Mirijello A., Ferrulli A., et al. Role of trait anxiety in persistent radicular pain after surgery for lumbar disc herniation: a 1-year longitudinal study. Neurosurgery. 2010; 67 (2): 265–71. https://doi.org/0.1227/01.NEU.0000371971.51755.1C.
30. Nayak N., Stephen J., Piazza M., et al. Quality of life in patients undergoing spine surgery: systematic review and meta-analysis. Global Spine J. 2019; 9 (1): 67–76. https://doi.org/10.1177/2192568217701104.
31. Lubelski D., Senol N., Silverstein M.P., et al. Quality of life outcomes after revision lumbar discectomy. J Neurosurg Spine. 2015; 22 (2): 173–8. https://doi.org/10.3171/2014.10.SPINE14359.
Об авторе
В. Н. БлохинаРоссия
Блохина Вера Николаевна, к.м.н.
ул. Нижняя Первомайская, д. 65, Москва 105203
Рецензия
Для цитирования:
Блохина В.Н. Оценка эффективности и безопасности ритмической периферической магнитной стимуляции у пациентов с пояснично-крестцовой радикулопатией в раннем реабилитационном периоде после микродискэктомии. Реабилитология. 2024;2(3):277–285. https://doi.org/10.17749/2949-5873/rehabil.2024.23
For citation:
Blokhina V.N. Efficacy and safety of repetitive peripheral magnetic stimulation in patients with lumbosacral radiculopathy during early postoperative rehabilitation period following microdiscectomy. Journal of Medical Rehabilitation. 2024;2(3):277–285. (In Russ.) https://doi.org/10.17749/2949-5873/rehabil.2024.23






